- نحوه ی دسترسی به پایان نامه های دانشگاه های مختلف جهان
- کاغذ لیتموس برای شناسایی غذاهای فاسد
- وجود سلنیم در خون مادر از ورود سم به بدن جنین جلوگیری میکند
- تعادل شیمیایی-شیمی تجزیه
- اثزدما بر تعادل-شیمی تجزیه رشته صنایع شیمیایی
- اثر دما بر انحلال پذیری-شیمی تجزیه رشته صنایع شیمیایی
- آدرس فیسبوک سایت
- چگونه برف درست کنيم
- دودزا
- نارنجک با پرمنگنات پتاسيم
آخرین مطالب
آنچه میخواهید در مورد CNG بدانید
گاز طبیعی سوختی با احتراق پاک، تمیز و بهینه است که سبب افزایش عمر موتور و کاهش تعمیرات آن میشود.
تعویض شمع در موتورهای بنزینی تا 32هزار کیلومتر دوام دارد ولی در موتورهای گازسوز این عدد به 120هزار کیلومتر افزایش مییابد.
این سوخت قابلیت انتقال و مکش از مخزن را ندارد و بدین ترتیب احتمال سرقت سوخت به صفر میرسد و این در حالی است که با توجه به سهمیهبندی بنزین، احتمال سرقت بنزین از باک خودروها وجود دارد.
زمان سوختگیری سریع در پمپ گاز بین 5 تا 6 دقیقه و آهسته آن 5 تا 8ساعت طول میکشد.
گاز طبیعی از بنزین ایمنتر است. چون گاز طبیعی برخلاف بنزین در زمان تصادف و حوادث پیشبینی نشده در هوا پراکنده میشود ولی بنزین روی زمین حوضچههایی ایجاد میکند که هر لحظه ممکن است به آتشسوزیهای مهیب منجر شود. کپسولهای ذخیره گاز هم بسیار محکمتر از تانکهای سوخت بنزینی هستند. طراحی این کپسولها منوط به اجرای شدیدترین آزمونهای ایمنی نظیر حرارت، فشارهای بسیار زیاد، تیراندازی و برخوردهای شدید است.
یک کیلوگرم گاز معادل 33/1لیتر بنزین و 22/1لیتر گازوئیل است.
رانندگی در ارتفاعات
در ارتفاعات، هوا رقیقتر شده و موتور با ترکیب سوخت غنیتری (نسبت بیشتری از سوخت به هوا) کار میکند. به همین خاطر قدرت موتور به دلیل کاهش تنفس موتور و تامین اکسیژن کمتر و همچنین جریان غنیتر و شدیدتر سوخت افت میکند. در این حالت چون موتور گازسوز به علت اینکه گاز در حدود 12درصد حجم ورودی را تشکیل داده و با کاهش چگالی هوا بر اثر رقیقتر شدن آن، حجم سوخت نیز پایین میآید، توان موتور 12 تا 14درصد افت میکند. پس در صورت دوگانهسوز بودن وسیله نقلیه بهتر است در ارتفاعات از سوخت بنزین استفاده شود.
عوامل موثر بر بازده سوخت
مقادیر ارزش حرارتی خالص بنزین، گازوئیل، LPG و CNG به ترتیب 46، 43، 45 و 44 است. تفاوت زیادی بین ارزش حرارتی خالص آنها وجود ندارد اما مقادیر ارزش حرارتی به میزان زیادی به ترکیب سوخت بستگی دارد.
در بسیاری از کشورها CNG دارای بهترین ارزش است. پس از آن گازوئیل، LNG و در نهایت بنزین قرار دارند.
چنانچه یک موتور بنزینی به سوخت CNG تبدیل شده باشد به بالاترین بازده دست پیدا نخواهد کرد چون ضریب تراکم در سطح مورد نیاز برای سوخت بنزین باقی میماند. بنابر این دستیابی به بالاترین راندمان فقط در خودروهای با موتورهای اصلی سوخت LNG امکان پذیر است. عموما احتمال آتش سوزی در شرایط عادی کارکرد، بسیار کم است. به علت سبکتر بودن گاز CNG نسبت به هوا، در فضا پراکنده میشود. اما بخار LPG از هوا سنگینتر است و به تشکیل حوضچه در نزدیکی زمین تمایل دارد. بر حسب قدرت، وسایل نقلیه دو گانه سوز (CNG) در حدود 10تا12درصد قدرت خود را به علت اینکه گاز طبیعی جای اکسیژن در محفظه احتراق موتور را میگیرد، از دست میدهند.
موتور گاز سوز داغتر از بنزین
موتورهای گاز سوز که از عملکرد بنزینی تبدیل به موتور گاز سوز شدهاند دارای اگزوزهایی با درجه حرارت بیشتر هستند. از طرفی در موتورهای بنزینی، بنزین تاثیر خنک کنندهای در سیستم مکش سوخت و سیلندرها دارد. این مساله در مورد گاز اتفاق نمیافتد. باید توجه داشت که یک مخلوط گازی تمایل به احتراق آهستهتری نسبت به بنزین دارد و ممکن است به هنگام عبور و خروج از سوپاپها باز هم در حال سوختن باشد.
کوبش موتورهای گازسوز
کارکرد موتور در شرایط جوی با درجه حرارت بالا، زمانبندی نادرست، احتراق تغییرات آنالیز و ترکیب شیمیایی گاز مهمترین علل کوبش در موتورهای گاز سوز هستند.
بنابراین این گاز طبیعی بادرصد متان بالا، کوبش موتورهای گاز سوز را تا حد زیادی کاهش میدهد.
سوالات عمومی در مورد CNG
این پرسشها توسط مردم در هنگام سوختگیری از پمپ گاز مطرح شدهاند. پاسخ به این پرسشها در جهت هر چه سریعتر شدن روند گازسوز کردن خودروها خالی از لطف نخواهد بود.
فرق گاز طبیعی با CNG چیست؟
CNG همان گاز طبیعی است که ما روزانه آن را در خانه، محل کار خود و یا کارخانجات با فشار پایین استفاده میکنیم. بدیهی است ذخیرهسازی گاز در چنین فشاری به واسطه حجم زیاد مورد نیاز به صرفه نیست. از طرفی به خاطر تراکم آن در صورت استفاده در خودرو، زمانهای تجدید سوختگیری فوقالعاده کوتاه خواهد شد. در صورتی که گاز طبیعی (NG) تا فشار حدود 3600PS تراکم شود، ما CNG خواهیم داشت.
آیا به هنگام استفاده از CNG، بوی گاز درون خودرو میپیچد؟
خوردوهای CNG سوز نظیر خودروهای بنزین سوز بدون بو هستند. در صورتی که در خودروهای CNG سوز بوی گاز احساس کردید، سریعا باید مدار سوخترسانی را از نظر نشست احتمالی مورد بازرسی قرار دهید.
تبدیل خودرو به CNGسوز چگونه تمام میشود؟
باک مخصوصی در صندوق عقب خودرو شما نصب میشود و مداراتی که بتواند گاز را در جهت احتراق به سمت موتورها هدایت کند، به آن مرتبط میشود.
در صورتی که ذخیره CNG در خودرو تمام شود، میتوان هنوز از بنزین استفاده کرد؟
بله، زمانی که شما خودروی مورد نظرتان را برای استفاده از CNG تبدیل میکنید، هنوز کاربراتور، باک بنزین و مدار سوخترسانی جهت بنزین را روی خودرویتان دارید. بنابراین به سادگی با زدن یک کلید روی داشبورد، میتوانید مسیر بنزین، به سمت موتور را برقرار کنید، اما به هر حال استفاده از CNG برای شما ارزانتر خواهد بود.
آیا لازم است که هر چند وقت یک بار حتی در صورت عدم نیاز اجباری از بنزین استفاده شود؟
بله این مساله، یعنی استفاده هر چند وقت یک بار از بنزین باعث روانکاری مکانیزم کاربراتور و آمادگی بهتر سیستم سوخترسانی بنزین در واقع لازم خواهد شد.
نصب کیت مخصوص و تبدیل خودرو به CNGسوز چقدر زمان میبرد؟
انجام این تبدیل 4 یا 5 ساعت بیشتر وقت نمیگیرد، اما افزایش روزافزون تقاضا برای انجام این تغییرات میتواند به واسطه ازدحام باعث طولانیتر شدن زمان انتظار مشتری شود.
با یک باک پر CNG، به طور معمول 10 تا 15لیتر بنزین، گاز طبیعی را در خود ذخیره میکند. بدیهی است اگر میزان مصرف خودرویتان را با واحد Km/Litr در این عدد ضرب کنید، میزان مسافت پیمودن با یک باک پر از CNG به دست میآید. برای مثال برای یک خودرو متوسط با حجم سیلندر 1300 سیسی این مسافت چیزی در حدود 155کیلومتر خواهد بود در صورت نیاز با افزودن تعداد باک میتوان این مسافت را افزایش داد.
آیا استفاده از گاز طبیعی فشرده در خودرو ایمن است؟
بله CNG به خاطر سه ویژگی مهم از سوختهای بنزین، گازوئیل و LPG ایمنتر است. اول آنکه وزن مخصوص CNG برابر 587/0 است این به آن معنا است که این گاز از هوا نیز سبکتر است. بنابراین در صورتی که نشست کند، در جو، صعود کرده و محو میشود. دوم اینکه درجه حرارت خوداشتغالی CNG برابر 700درجه سانتیگراد است، در حالی که درجه حرارت خوداشتغالی بنزین 455درجه سانتیگراد است. سومین مورد، این که باکهای ذخیره CNG از فولادهای آلیاژی خاص و با رعایت بالاترین سطوح ایمنی ساخته میشوند که بسیار محکمتر و ایمنتر از باکهای بنزین خودروها هستند.
آیا باک ذخیره CNG در خودرو با چنین فشار بالای گاز درون آن ایمن است؟
بله، باکهای ذخیره CNG از فولادهای آلیاژی خاص و به صورت کاملا یکپارچه ساخته میشوند. هیچ نوع جوشی در ساخت این باک به کار نرفته و باک براساس استانداردهای معتبر بینالمللی قبل از نصب مورد تست قرار میگیرد. بهعلاوه این باکها به دیسکهای پارهشونده ضدانفجار (Burst disc) مجهز هستند که در صورت افزایش بیش از حد فشار یا به هنگام آتشسوزی این دیسکها پاره شده و فشار مخزن به شدت افت کرده و بخش اعظم گاز خارج میشود.
آیا وجود باک ذخیره پرفشار گاز در خودرو حتی به هنگام تصادفهای شدید نیز ایمن است؟
CNG سالها است که در کشورهایی چون نیوزیلند، ایتالیا، آرژانتین و آمریکا به عنوان سوخت خودروها مورد استفاده قرار میگیرد و تمام این کشورها آن را ایمنتر از بنزین شناخته و اعلام کردهاند.
آیا استفاده از CNG برای موتور خودرو ضرری نداشته و به آن آسیب نمیزند؟
خیر به هیچ عنوان بالعکس عمر برخی از قطعات موتور در صورت استفاده CNG افزایش خواهد یافت. به عنوان مثال عمر مفید روغن موتور تا حد زیادی افزایش مییابد، چرا که CNG باعث آلودگی یا رقیق شدن روغن موتور نمیشود. از طرفی چون هیچگونه سربی به همراه این سوخت نیست رسوبات سخت سرب روی شمعها ایجاد نشده و عمر مفید شمعها نیز تا حد چشمگیری افزایش مییابد. همچنین از آنجا که CNG سوختی گازی است، هیچ کربنی به عنوان محصول احتراق تشکیل نشده و سطح داخلی موتور تمیز باقی میماند.
چرا دود و دمه خروجی از اگزوز خودروهای CNG سوز کم و محدود است؟
زیرا CNG در عمل سوختی پاک و تا حد بسیار زیادی عاری از آلایندههای زیست محیطی است از انجام که عمده ترکیب اصلی گاز طبیعی را متان تشکیل میدهد خروجی اگزوز خودروهای CNG سوز شامل بخار آب و جز کوچکی مونوکسید کربن است.
با توجه به اینکه کربن یا ذرات دیگری در خروجی اگزوز وجود ندارد دود خروجی از اگزوز بسیار جزئی و قابل اغماض است. به دلایل فوق خودروهای CNG سوز به راحتی و بدون به کارگیری هر نوع تجهیزات جانبی و خارجی (نظیر مبدلهای کاتالیستی در خودروهای بنزینی سوز)ف قادر خواهند بود برآورده کننده کلیه الزامات مشخص شده در استانداردهای زیست محیطی باشند.
عملکرد و کارایی CNG در مقایسه با بنزین در یک خودروی تبدیل شده به دوگانهسوز چگونه است؟
هنگام استفاده از CNG شتاب حرکت خودرو در مقایسه با بنزین اندکی کمتر خواهد بود که این مساله به واسط افت 5 تا 15درصدی قدرت موتور به هنگام استفاده از CNG است. شایان ذکر است این میزان افت توان موتور را میتوان با تنظیم کیت CNG به حداقل رساند و در شرایط معمول رانندگی در شهر این میزان افت قدرت، محسوس نخواهد بود.
آیا تجهیزات و سیستم سوخترسانی CNG نصب شده روی خودرو نیاز به تعمیر یا سرویس خاصی دارد؟
به طور کلی این سیستم سوخترسانی سیستم پیچیدهای نیست و به راحتی میتواند سالها بدون اشکال کار کند اما برای آنکه همواره در شرایط حداکثر کارایی خود قرار داشته باشد بازدید دورهای تجهیزات مربوط به آن بعد از هر یکهزار کیلومتر کارکرد پیشنهاد میشود که ترجیحا میباید نزد همان تکنسین مجازی که خودرو را گازسوز کرده انجام شود.
آیا خودروهای دیزل را نیز میتوان CNG سوز کرد؟
بله میتوان خودروهای دیزل را هم به CNG سوز هم به دوگانهسوز (Dual Fuel) برای مصرف CNG و گازوئیل تبدیل کرد.
با وجود مزایای بسیار استفاده از CNG چرا کشورهای توسعه یافته از آن استفاده نمیکنند؟
بد نیست بدانیم که CNG در سطح جهان سوخت جدیدی نیست و خودروها از دهه 1920 میلادی تاکنون از این سوخت استفاده کردهاند. در حال حاضر ایتالیا 240 جایگاه عرضه CNG، بیش از 300هزار خودروی CNG سوز دارد. در نیوزیلند نیز حدود 250هزار خودرو در سالهای اخیر CNG سوز شدهاند و حدود 250 جایگاه، عرضه CNG در این کشور را بر عهده دارند. آرژانتین نیز در چند ساله اخیر برنامهریزی گستردهای را برای استفاده CNG طرحریزی کرده و در حال حاضر 700هزار خودروی CNG سوز دارد. سومین مورد اینکه باکهای ذخیره CNG از فولادهای آلیاژی خاص و با رعایت بالاترین سطح ایمنی ساخته میشوند که بسیار مستحکمتر و امنتر از پلاکهای بنزین خودروها هستند .
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 303 تاريخ : جمعه 20 اسفند 1389 ساعت: 18:18
آلودگی هوا
تعدادی از اکسیدها که به مقادیر مختلف در هوا وجود دارند ، به محیط زیست زیان می رسانند . تمدن امروز مواد بیگانه ای را به میزان روز افزون وارد جو می کنند . مواد زیان بخش زاید به ترتیب مقدار عبارتند از :
مونواکسید کربن
کربن مونوکسید، (با فرمول شیمیایی CO)، گازی است که بر اثر ناقص سوختن کربن بوجود میآید. این گاز بسیار سمی است اما رنگ و بوی خاصی ندارد.
تمامی وسایل و دستگاههایی که وظبفه سوزاندن چیزی را دارند (مانند یک بخاری گازی یا نفتی، یک آبگرمکن و یا حتی موتور یک خودرو) تا حدودی مونواکسیدکربن تولید میکنند، میزان این تولید به شرایط احتراق (سوختن) بستگی دارد؛ هرچه میزان اکسیژن در هنگام سوختن کمتر باشد بخش بیشتری از کربنها دچار ناقص سوزی میشوند و به جای کربن دیاکسید (CO۲) مونواکسیدکربن تولید میکنند.
افرادی که در یک فضای سربسته در معرض استنشاق این گاز قرار میگیرند ابتدا احساس کرختی و خواب آلودگی میکنند و در صورتی که هرچه سریعتر مکان را ترک نکنند و یا هوای تازه تنفس نکنند دچار بیهوشی و در نهایت خفگی میشوند.
برای دوری از خطرات همین گاز است که مدام توصیه میشود برای بخاریهای گازی منازل حتماً از دودکشهای کلاهک دار استفاده شود.
دی اکسید گوگرد
گوگرد دیاکسید یک ترکیب شیمیایی به شکل گاز در دمای اتاق با فرمول SO2 میباشد. این ماده توسط آتشفشانها و بسیاری از فعالیتهای صنعتی تولید می شود. سوختن نفت و ذغال سنگ به علت وجود ترکیبات گوگردی در آنها با تولید این گاز همراه است. معمولاً کاتالیزگرهایی چون NO2 در جو باعث واکنش این گاز با بخار آب موجود در هوا و تشکیل اسید سولفوریک می شود. این گاز بی رنگ سمی دارای جرم مولی ۶۴٫۰۷ گرم بر مول، چگالی ۲٫۵۵۱ گرم بر لیتر، نقطهٔ ذوب ۷۵٫۵- درجهٔ سانتی گراد و نقطهٔ جوش ۱۰٫۰- درجهٔ سانتی گراد است و اشتعال زا نیست.
مونو اکسید نیتروژن
مونوکسید دی نیتروژن یا نیتروز اکساید یا گاز خنده (N2O) یکی از ترکیبات نیتروژن میباشد که اولین بار در سال ۱۷۹۹ در دندانپزشکی استفاده شد. امروزه از آن در پزشکی برای القاء و ادامه بیهوشیمصرف میشود. این دارو همچنین بامقادیر مصرف کم بهعنوان ضد درد دراعمال جراحی زنان و زایمان و برای اعمالجراحی که در آنها به بیهوشی کامل بیمار نیاز نیست، مصرف میشود.
نیتروژن اکسید (N۲O) گازی بی رنگ، بی بو و غیر قابل اشتعال است. N۲O سمی نیست اما خنده آور است.
هیدروکربن ها
گرچه استانداردهای ملی کیفیت هوا اصولاً در سال 1971 برای هیدروکربنهای غیرمتانی تصویب شد، اما تا سال 1983 که بازنگری گستردهای روی آن انجام گرفت، عملاً مورد استفاده قرار نگرفت. هیدروکربنها همراه با اکسیدهای نیتروژن در حضور نور آفتاب موجب تشکیل اکسیدانهای فتوشیمیایی، از جمله ازون میشوند که اثرات مخربی روی سلامت انسان و روی گیاهان دارند. بدین دلیل اعتقاد بر این بود که تدوین استاندارد برای ازون مناسبتر از استاندارد برای هیدروکربنهاست.
مطالعات انجام شده بر روی تاثیر بسیاری از هیدروکربنهای گازی با غلظتهای موجود در آتمسفر اثر تخریبی و مستقیم آنها را بر سلامت انسان ثابت نمیکند. بررسیها در مورد سرطانزایی گروههای هیدروکربنه معین نشان میدهد که برخی سرطانها به علت مجاورت با هیدروکربنهای آروماتیک موجود در دوده و قیر، ظاهر شدهاند. برخی ذرات سرطانزا، از جمله هیدروکربنهای آروماتیک چند هستهای در هوای آزاد قابل تشخیص هستند.
گروه گسترده هیدروکربنهای گازی اغلب از نظر خورندگی اثر قابل سنجشی روی مواد باقی نمیگذارند. از بین تمام هیدروکربنها، تنها اتیلن در غلظتهای شناخته شده در هوای تنفسی، اثرات نامطلوبی روی گیاهان دارد. اثر اصلی اتیلن، بازدارندگی در رشد گیاهان است. اتیلن با غلظتهای ppm ٠.٠٠١ تا ٠.۵ سببتحریک گیاهان حساس از جمله افتادگی گلها و عدم بازشدن درست برگها میشود. ایجاد صدمه به گلهای ارکیده و پنبه به اثبات رسیده است.
با وجود آنکه در حال حاضر هیدروکربنها در یک گروه کلی از آلایندهها جزء فهرست آلایندههای اصلی قرار نگرفته اند ، تعداد زیادی از ترکیبات هیدروکربنه خاص در بین 189 آلاینده خطرناکی هستند که تحت نام تبصره مواد سمی هوا در قانون هوای پاک مصوب 1990 قرار دارند.
هیدروکربن های هالوژن دار
هیدروکربنهای دارای کلرفلوئر برم و ید(هالوژنها) باهیدروکربنهای نفتی تفاوت دارند چراکه اکثر انها براحتی طی اکسیداسیون شیمیایی یا فعالیت باکتریایی تجزیه نمی گردند.
هیدروکربنهای دارای کلرفلوئر برم و ید(هالوژنها) باهیدروکربنهای نفتی تفاوت دارند چراکه اکثر انها براحتی طی اکسیداسیون شیمیایی یا فعالیت باکتریایی تجزیه نمی گردند.مشابه فلزات الاینده های پایدار بوده واضافات دائمی در محیط زیست دریایی هستند.برخلاف فلزات بیشتر انها ساخته دست انسان بوده وبصودژرت طبیعی وجود ندارندو درضمن در رسوبات وبدن جانوران مجتمع میشوند.اکثریت بزرگی از انها حاوی کلر هستند وتحت عنوان هیدروکربنهای کلردارشناخته می شوند.
ذرات ریز معلق
يك مطالعه جديد نشان ميدهد استنشاقذرات ريز فلزات موجود در آلايندههاي هوا احتمال ابتلا به سرطان ريه را افزايش ميدهد. محققان با بررسي موارد سرطان ريه در تگزاس ارتباطي را بين فلزات موجود در ذرات ريز معلق در هوا و ميزان ابتلا به سرطان ريه "آدنوكارسينوما" يافتند. اين نوع سرطان اغلب زنان غيرسيگاري را مبتلا ميكند. دكتر ايوون كويل استاديار طب داخلي در مركز پزشكي "يوتيساوت وسترن" در دالاس ميگويد اين تحقيق به روشن شدن علت بروز سرطان ريه در زنان به ويژه زنان غيرسيگاري كمك ميكند.
كويل و همكارانش از سال ۱۹۹۵تا ۲۰۰۰بيش از ۸۰هزار مورد سرطان ريه را در ۲۵۴منطقه تگزاس شناسايي كردند و نتايج را با اطلاعات آلودگي هواي صنعتي كه طي سالهاي ۱۹۸۸تا ۲۰۰۰به سازمان حفاظت محيط زيست آمريكا گزارش شده بود مقايسه كردند.
اين مقايسه نشان داد ميزان بروز سرطان در مناطقي كه بيشترين آلودگي را دارد شايعتر است و در مناطقي كه آلودگي كمتر است ميزان سرطان نيز پايينتر است.
ذرات معلق در هوا كه از ذرات بسيار كوچك گرد و غبار و آب تشكيل شده است در اثر سوزاندن سوختهاي فسيلي كه معمولا با فرايندهاي صنعتي يا خودروها ارتباط دارد وارد جو زمين ميشود.
كوچكترين اين ذرات PM 2.5نام دارد و حاوي فلزات سنگين است. ضخامت اين ذره دو و نيم ميكرومتر است كه ۱۰۰بار از موي انسان نازكتر است. تحقيقات قبلي نشان داده است اين ماده در بروز سرطان ريه نقش دارد.
سازمان حفاظت محيط زيست اين ماده را يكي از شش آلاينده در قانون هواي پاك قرار داده است و حد مجازي براي آن تعيين كرده كه هر پنج سال يكبار اين سازمان استانداردها را به روز ميكند.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 302 تاريخ : پنجشنبه 19 اسفند 1389 ساعت: 10:52
واژه نانوفیلتراسیون تا اواسط نیمه دوم دهه 80 هنوز به طور مشخص مورد استفاده قرار نگرفته بود. در حقیقت این غشاها از اوایل دهه 60 وجود داشتند و با عناوین غشاهای اسمز معکوس آزاد(Loose Reverse Osmosis)، اسمز معکوس باز(Open Reverse Osmosis)، حد واسط غشاهای اسمز معکوس و اولترافیلتراسیون،غشاهای اسمز معکوس انتخابی(Selective Reverse Omosis) و یا غشاهای اولترافیلتراسیون فشرده(Tight Ultrafiltration) مورد استفاده قرار می گرفت. بنابراین تولید نانوغشاها با تولید غشاهای اسمز معکوس و اولترافیلتراسیون همزمان بوده و به اواخر دهه 50 تا اول دهه 1960 برمی گردد. طی مدت زمان نزدیک به 15 سال، به موجب توسعه و پیشرفت فناوری در زمینه غشاهای اسمز معکوس و اولترافلتراسیون و کشف پتانسیل های بالقوه کاربرد فرایندهای غشایی در صنایع مختلف، منجر به ایجاد غشاهای جدید از نوع نانو شد.
تعریف نانوفیلتراسیون
به طور معمول جداسازی نمک های تک ظرفیتی، دو ظرفیتی و حل شده های غیریونی با وزن مولکولی کمتر از 2000 گرم بر مول، عامل اصلی در انتخاب غشاهای جدید با خواص و ویژگی های فی مابین غشاهای اسمز معکوس و اولترافیلتراسیون می باشد. محدوده ویژگی ها و مشخصات فرایند جداسازی غشاهایی که از طریق این تعریف پوشش داده می شود به تازگی به عنوان غشاهای نانو مطرح شده است.
این فرایند در سال های 1980 نیز تحت عنوان هیپرفیلتراسیون (Hyperfiltration) از آن نام برده شده و همیشه همراه با فرایند اسمز معکوس و مشابه آن معرفی شده است. امروزه نانوفیلتراسیون به صورت یک فرایند به طور کامل مجزا با خواص کاربردی ویژه به کار گرفته می شود و با دو فرآیند اسمز معکوس و اولترافیلتراسیون اختلاف های اساسی دارد. به عبارتی غشاهای به کار رفته در فرایند نانوفیلتراسیون دارای ساختار متخلخل از نوع میکرو با قطر روزنه های کمتر از 2 نانومتر بوده و از مواد پلیمری، که در بیشتر حالت ها دارای بار یونی می باشند، ساخته شده اند.
شهرت تجاری نانوفیلتراسیون از اوایل سال های 1980 آغاز شده و در سال 1988 اولین نانوغشاها از جنس مواد سرامیکی به صورتتجاری و کاربردی مورد استفاده قرار گرفت. بعدها نانوغشاهایی از جنس مواد پلیمری آلی جهت کاربردهای خاص به بازار عرضه شد.
در حال حاضر غشاهای نانو در بخش های مختلف صنایعی چون بیوتکنولوژی، صنایع غذایی و کشاورزی، تولید آب آشامیدنی و حفاظت محیط زیست به طور گسترده ای مورد استفاده قرار می گیرد. برای مثال، می توان به جداسازی مواد معدنی از لاکتوز در صنایع شیر، بازیابی و استفاده مجدد از آب مصرفی در پساب های رنگی و تصفیه آب شرب در یک مقیاس بزرگ اشاره کرد.
کاربردهای ممکن فرایند نانوفیلتراسیون در صنایع مختلف
غذایی:
- نمک زدایی از محلول پنیر
- نمک زدایی از محلول شکر
- بازیابی مواد غذایی در فرایند تخمیر
- تصفیه پساب
- خالص سازی اسیدهای آلی
نساجی، چرم و کاغذ:
- جداسازی اسیدهای آمینه
- بازیابی رنگینه ها از پساب
- بازیابی آب و نمک از پساب
- بازیابی مواد آهاری از پساب آهارگیری
- بازیابی و استفاده مجدد از یون های کروم
- تصفیه پساب
شیمیایی:
- بازیابی محلول سفیدگری
- حذف گاز دی اکسیدکربن در فرایند گازی
- تهیه برومید
- بازیابی قلیا در فرایند تولید سلولز و ویسکوز
- رسوب سولفات کلسیم
الکترونیک و آّبکاری:
- جداسازی فلزات سنگین از محلول اسیدها
- حذف سولفات های فلزی از پساب
- حذف نیکل
تولید آب:
- بازیابی هیدروکسید لیتیم در تصفیه پساب باتری سازی
- حذف مواد روغنی از آب
- حذف سختی از آب
- حذف مواد آلی طبیعی
- حذف سموم دفع آفات از آب
- حذف فلزات سنگین، آهن، مس، روی و سیلیکا
- تصفیه آب های شور
کشاورزی:
- حذف فسفات، سولفات، نیترات و فلوراید
- حذف سلنیوم از آب زهکشی
ویژگی ها و مشخصات اصلی و اساسی فرایند نانوفیلتراسیون عبارتند از:
- جرم مولکولی ذرات و مولکول های احتباس شده توسط این غشا بین 200 تا 2000 گرم بر مول (دالتون) قرار می گیرد.
- میزان احتباس ذرات باردار تابع بار یونی آن ها می باشد نه جرم مولکولی آن ها
- محدوده فشار اعمال شده در این فرایند در مقایسه با فرایند اسمز معکوس کمتر و بالعکس دبی جریان عبوری از غشا به مراتب بیشتر از دبی به دست آمده از فرایند اسمز معکوس در یک فشار ثابت می باشد.
- دبی جریان خروجی و عبوری از غشاهای نانو براساس آنالیز تئوری های دو پدیده نفوذ و جابجایی قابل توصیف است.
به دلیل استفاده از پلیمرهای یونی در ساخت غشاهای نانو، احتباس ذرات یونی از مکانیزم اثر دافعه دونان (Donnan Exclusion) تبعیت می کند. بررسی جزییات مکانیزم های انتقال مواد در غشا نشان می دهد که این نوع مکانیزم از ویژگی های خاص غشاهای نانو در مقایسه با دو نوع غشای اسمز معکوس و اولترافیلتراسیون می باشد.
در نانوغشاها یک انتخاب در احتباس بین یون های تک ظرفیتی و دوظرفیتی وجود دارد. به عبارت دیگر توسط فرایند نانوفیلتراسیون امکان جداسازی یون های یک ظرفیتی از دوظرفیتی وجود دارد. در حالی که علی رغم احتباس خیلی زیاد فرایند اسمز معکوس، این نوع جداسازی به وسیله غشاهای اسمز معکوس وجود ندارد.
همچنین در غشاهای نوع نانو اختلاف بسیار مهمی در نفوذپذیری بین دو ذره ای که از نظر جرم مولکولی یکسان ولیکن دارای بارهای یونی مخالف (مثل یک ذره یونی مثبت یا منفی، و یک ذره خنثی) هستند، وجود دارد. در حالی که چنین اختلافی در دو نوع غشای اسمز معکوس و اولترافیلتراسیون دیده نمی شود.
ساختار نانوغشاها
غشاهای استفاده شده در فرآیند نانوفیلتراسیون، برحسب ماهیت آلی یا معدنی، از پلیمرها و یا اکسیدهای فلزی ساخته شده اند و دارای یک ساختار اسیمتریک هستند. یک نانوغشا از سه لایه، که هر یک نقش ویژه ای دارد تشکیل شده است:
- یک لایه اولیه با قطر روزنه های بزرگتر از 50 نانومتر به منظور دادن مقاومت مکانیکی خوب به غشا و امکان کسب دبی جریان عبوری بالا.
- یک یا چندین لایه میانی با قطر منافذ بین 2 و 50 نانومتر که ارتباط بین لایه حفاظتی و لایه فعال را مطمئن می سازد.
- یک لایه فعال که توسط آن عمل جداسازی توسط فرآیند نانوفیلتراسیون انجام می شود. ضخامت این لایه به نسبت کم بوده و اغلب در حدود کمتر از میکرون با قطر روزنه های در مقیاس نانومتر می باشد. توزیع اندازه این روزنه ها خیلی باریک می باشد. این لایه ضمن داشتن دبی جریان عبوری بالا، دارای ویژگی خاص در انتخاب فرآیند جداسازی بین ذرات یونی و غیریونی، که جرم مولکولی آن ها کمتر از 2000 گرم بر مول است، می باشد.
فراتر از این ساختار عمومی و کلی، غشاهای نانو از خصوصیت های فیزیکی و شیمیایی ویژه ای در ارتباط با ماهیت آلی یا معدنی خود برخوردار هستند.
مشخصه های غشاهای پلیمری آلی
غشاهای نانو ساخته شده از مواد پلیمری آلی، مشابه غشاهای اسمز معکوس، دارای یک ساختار کمپوزیت بوده که طی یک فرآیند دو مرحله ای به شرح زیر ساخته می شوند:
- ابتدا یک لایه پلیمری متخلخل با قطر روزنه های بزرگتر از 50 نانومتر به ضخامت بین 40 تا 100 میکرومتر به صورت لایه میانی روی یک منسوج بافته شده یا بی بافت قرار می گیرد.
- سپس یک لایه فعال با ضخامت کم، بین 0.3 تا 3 میکرومتر توسط فرآیندهایی چون پلیمریزاسیون روی لایه قبلی ایجاد می شود. این لایه فعال خواص انتقال و انتخاب در جداسازی را برای نانوغشا ایجاد می کند.
لایه میانی آن ایزوتروپ (Anisotrope)بوده که اغلب بر پایه پلی سولفون می باشد. این لایه دارای نفوذپذیری بسیار بالایی است. بعضی از غشاها ممکن است دارای چندین لایه میانی باشند.
لایه فعال باید علاوه بر داشتن احتباس ویژه در فرآیند جداسازی، از مقاومت مکانیکی و شیمیایی خوبی برخوردار باشد. به عنوان مثال بعضی از لایه های فعال از طریق پلیمریزاسیون بین سطحی توسط ترکیبات آروماتیک سه عاملی روی لایه میانی ایجاد می شوند.
در دیدگاه اول، توانایی جداسازی لایه فعال، تحت اثر یک سد فیزیکی ایجاد شده توسط غشا، در نظر گرفته می شود که عبور از این غشا تابع اندازه مولکولی ذرات است. به عبارت دیگر ذراتی که دارای قطر کمتر از قطر روزنه های لایه فعال هستند می توانند از این لایه عبور کرده و در نتیجه ذرات بزرگ تر احتباس می شوند.
توانایی جداسازی نانوغشا با اثر بار یونی که ناشی از ماهیت شیمیایی پلیمرهایی که در ساخت این لایه فعال استفاده می شوند ارتباط دارد. در حقیقت در بین مواد سازنده ای که تشکیل دهنده لایه فعال غشاهای نانو می باشند، گروههای فعال چون آمید، کربوکسیل و حتی سولفون وجود دارد. این گروهها ممکن است یا به طور دائم و یا تابع محلولی که در تماس با این غشا خواهد بود، به صورت یونی باردار شوند.
مشخصه های غشاهای معدنی
نانوغشاهای معدنی یا سرامیکی دارای یک ساختاری مشابه غشاهای معدنی از نوع میکروفیلتراسیون و اولترافیلتراسیون هستند. تنها اختلاف آن ها در لایه نهایی است. این لایه در نانوغشاهای معدنی دارای ساختار متخلخل با اندازه حفره های میکرو یعنی قطر منافذ کمتر از 2 نانومتر می باشد.
از نظر اصول اولیه، ساختار چند لایه ای غشاهای سرامیکی مشابه ساختار نانوغشاهای پلیمری است. به طور عمومی این لایه های فعال در نانوغشاهای معدنی توسط فرآیند سل-ژل به دست می آیند.
فرآیند سل-ژل یکی از فرآیندهای شیمیایی است که در دمای پایین برای تولید اشیاء، فیلم ها، فیبرها، ذرات یا کمپوزیت ها مناسب می باشد که می توانند بعد از یک مرحله فرآیند تکمیلی به صورت تجاری مصرف شوند. به وسیله فرآیند سل-ژل می توان ساختار میکرو محصولات را در محدوده 1 تا 100 نانومتر که ساختاری در مرتبه مولکولی می باشد به دست آورد. این مواد اغلب مشخصه های فیزیکی و شیمیایی یکنواختی دارند. سل ها ذرات کلوئیدی پراکنده در محلول به ابعاد 100-1 نانومتر هستند که به علت کوچکی بیش از حد به وسیله حرکت براونی در محلول به حالت معلق باقی می مانند. ژل ها نیز از یک شبکه جامد و به هم پیوسته با منافذی به ابعاد زیر میکرومتر و زنجیرها پلیمری می باشند که طول متوسط آن ها بزرگتر از یک میکرومتر است. در حقیقت فرآیند سل-ژل سنتز شبکه معدنی توسط واکنش های شیمیایی در محلول و در دمای پایین است که به دلیل تشکیل شبکه بی شکل (در مراحل اولیه) در مقابل فرآیند کریستاله شدن در محلول قرار دارد.
در این فرآیند برای تهیه نانوغشا اغلب از اکسیدهای فلزی، که از محلول فلزات آلی یا نمک های معدنی حاصل می شود، استفاده می گردد. سپس لایه های نازک با تخلخل قابل کنترل توسط نانوذرات اکسیدهای مواد معدنی با قطر کمتر از 10 نانومتر تشکیل می شود.
یکی از ویژگی های مهم اکسیدهای معدنی یاد شده، خاصیت آمفوتر بودن آن ها می
باشد،همچنین پدیده هیدراسیون در سطح غشا و روی دیواره حفره های غشا انجام می شود. پدیده هیدراسیون علت تشکیل بارهای الکتریکی در سطح شده که تابعی از محتویات محلولی است که با غشا در تماس می باشد.
برای هر اکسید یک محدوده pH وجود دارد که در آن بارهای مثبت و منفی سطح غشا با هم برابر است و در مجموع سطح از نظر بار الکتریکی خنثی است. این نقطه از pH را در اصطلاح نقطه بار صفر گویند. این محدوده pH به نوع اکسید و همچنین درجه حرارتی که هنگام ساخت غشا به مواد وارد شده است، بستگی دارد. شناخت این محدوده pH برای اکسیدهای فلزی یک پارامتر مهم محسوب می شود و در واقع این پارامتر رفتار نانوغشاهای سرامیکی را در مقابل محلول نشان می دهد. هنگامی که اکسید فلزی در تماس با محلول های یونی قرار می گیرد، یون های با بار مخالف لایه فعال غشا جذب سطح شده و تولید یک لایه ثانویه می کند. این لایه را لایه استرن (Ste layer) گویند. در محدوده ای از pH برآیند بارهای الکتریکی موجود در سطح پس از جذب یون های مخالف و تشکیل لایه ثانویه تولید یک سطح در مجموع خنثی می کند. این نقطه pH را نقطه ایزوالکتریک می گویند. پایین تر از نقطه pH ایزوالکتریک، سطح در مجموع به صورت مثبت و بالاتر از آن به صورت منفی باردار خواهد بود. از نظر علمی برای توصیف رفتار غشاها در تماس با محلول های واقعی، نقطه ایزوالکتریک ارجحیت بیشتری نسبت به نقطه بار صفر دارد.
منبع :http://forum.p30world.com/showthread.php?t=448334
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 362 تاريخ : جمعه 6 اسفند 1389 ساعت: 10:6
ترمودینامیک شیمیایی
تعیین سمت و سوی واکنش
ترمودینامیک شیمیایی در عمل ، برقراری چهارچوبی برای تعیین امکان پذیربودن یا خود به خود انجام شدن تحولی فیزیکی یا شیمیایی معین است. به عنوان مثال ، ممکن است به حصول معیاری جهت تعیین امکان پذیر بودن تغییری از یک فاز به فاز دیگر بطور خود به خود مانند تبدیل گرافیت به الماس یا با تعیین سمت و سوی خود به خود انجام شدن واکنشی زیستی که در سلول اتفاق میافتد، نظر داشته باشیم.
در حلاجی این نوع مسائل ، چند مفهوم نظری و چند تابع ریاضی دیگر بر مبنای قوانین اول و دوم ترمودینامیک و برحسب توابع انرژی گیبس ابداع شدهاند که شیوههای توانمندی برای دستیابی به پاسخ آن مسائل ، در اختیار قرار دادهاند.
تعادل
پس از تعیین شدن سمت و سوی تحولی طبیعی ، ممکن است علم بر میزبان پیشرفت آن تا رسیدن به تعادل نیز مورد توجه باشد. به عنوان نمونه ، ممکن است حداکثر راندمان تحولی صنعتی یا قابلیت انحلال دیاکسید کربن موجود در هوا ، در آبهای طبیعی یا تعیین غلظت تعادلی گروهی از متابولیتها ( Metabolites ) در یک سلول مورد نظر باشد. روشهای ترمودینامیکی ، روابط ریاضی لازم برای محاسبه و تخمین چنین کمیتهایی را بدست میدهد.
گرچه هدف اصلی در ترمودینامیک شیمیایی ، تجزیه و تحلیل در بررسی امکان خود به خود انجام شدن یک تحول و تعادل میباشد، ولی علاوه بر آن ، روشهای ترمودینامیکی به بسیاری از مسائل دیگر نیز قابل تعمیم هستند. مطالعه تعادلهای فاز ، چه در سیستمهای ایده آل و چه در غیر آن ، پایه و اساس کار برای کاربرد هوشمندانه روشهای استخراج ، تقطیر و تبلور به عملیات متالوژی و درک گونههای کانیها در سیستمهای زمین شناسی میباشد.
تغییرات انرژی
همین طور ، تغییرات انرژی ، همراه با تحولی فیزیکی یا شیمیایی ، چه به صورت کار و چه به صورت گرما مورد توجه جدی قرار دارند؛ این تحول ممکن است احتراق یک سوخت ، شکافت هسته اورانیوم یا انتقال یک متابولیت در بستر گرادیان غلظت باشد.
مفاهیم و روشهای ترمودینامیکی ، نگرشی قوی برای درک چنان مسائلی را فراهم می آورد که در شیمی فیزیک مورد بررسی قرار میگیرند.
الکتروشیمی
تمام واکنشهای شیمیایی ، اساسا ماهیت الکتریکی دارند؛ زیرا الکترونها ، در تمام انواع پیوندهای شیمیایی (به راههای گوناگون) دخالت دارد. اما الکتروشیمی ، بیش ار هر چیز بررسی پدیده های اکسایش- کاهش (Oxidation - Reduction) است. روابط بین تغییر شیمیایی و انرژی الکتریکی ، هم از لحاظ نظری و هم از لحاظ عملی حائز اهمیت است.
از واکنشهای شیمیایی میتوان برای تولید انرژی الکتریکی استفاده کرد، (در سلولهایی که "سلولها یا پیلهای ولتایی" یا "سلولهای گالوانی" نامیده میشوند) و انرژی الکتریکی را میتوان برای تبادلات شیمیایی بکار برد (در سلولهای الکترولیتی). علاوه بر این، مطالعه فرایندهای الکتروشیمیایی منجر به فهم و تنظیم قواعد آن گونی از پدیده های اکسایش- کاهش که خارج از این گونه سلولها یا پیلها روی می دهد نیز میشود.
سینتیک شیمیایی (Chemical Kinetic)
سینتیک شیمیایی عبارت از بررسی سرعت واکنشهای شیمیایی است. سرعت یک واکنش شیمیایی را عوامل معدودی کنترل میکنند. بررسی این عوامل ، راههایی را نشان میدهد که در طی آنها ، مواد واکنشدهنده به محصول واکنش تبدیل میشوند. توضیح تفضیلی مسیر انجام واکنش بر مبنای رفتار اتمها ، مولکولها و یونها را "مکانیسم واکنش" مینامیم.
در ترمودینامیک و الکتروشیمی ، کارها پیشبینی انجام واکنش بود؛ اما مشاهدات صنعتی ، نتایج ترمودینامیک شیمیایی را به نظر تایید نمیکند. در این حالت نبایستی فکر کنیم که پیش بینی ترمودینامیک اشتباه بوده است؛ چون ترمودینامیک کاری با میزان پیشرفت واکنش و نحوه انجام فرایندها ندارد. نظر به اهمیت انجام فرایندها از نظر بهره زمانی ، لازم است که عامل زمان در بررسی فرایندها وارد شود.
به عنوان مثال ، کاتالیزورهای بخصوصی به نام "آنزیمها" در تعیین این که کدام واکنش در سیستمهای زیستی با سرعت قابل ملاحظه به راه بیافتد، عواملی مهم هستند. مثلا مولکول "تری فسفات آدنوزین" (Adnosine triphosphate) از لحاظ ترمودینامیکی در محلولهای آبی ناپایدار بوده و باید هیدرولیز گردیده و به "دی فسفات آدنوزین" و یک فسفات معدنی تجزیه شود. در صورتی که این واکنش در غیاب آنزیمی ویژه ، "آدنوزین تری فسفاتاز" ، بسیار کند میباشد.
در واقع همین کنترل ترمودینامیکی سمت و سوی واکنشها به همراه کنترل سرعت آنها توسط آنزیمهاست که موجودیت سیستمی با تعادل بسیار ظریف ، یعنی سلول زنده را مقدور میسازد. بیشتر واکنشهای شیمیایی طی مکانیسمهای چند مرحلهای صورت میگیرند. هرگز نمیتوان اطمینان داشت که یک مکانیسم پیشنهاد شده ، بیانگر واقعیت باشد. مکانیسم واکنشها تنها حدس و گمانهایی بر اساس بررسیهای سینتیکیاند.
ارتباط شیمی فیزیک با سایر علوم
همانطور که عنوان شد و از نام شیمی فیزیک پیداست، این علم ، مسائل و پدیدههای شیمیایی را با اصول و قوانین فیزیک توجیه میکند و ارتباط تنگاتنگی میان شیمی و فیزیک برقرار میکند. علاوه بر آن ، روابط بسیار پیچیده شیمیایی با زبان ریاضی ، مرتب و طبقهبندی شده و قابل فهم میگردد. بسیاری از پدیدههای زیستی مانند سوخت و ساز مواد غذایی در سلولهای بدن با علم شیمی فیزیک توجیه میشود و این ، ارتباط شیمی فیزیک را با زیست شناسی و به تبع آن پزشکی بیان میکند.
بسیاری از پدیده های طبیعی که به صورت خود به خودی انجام میگیرد، همانند تبدیل خود به خودی الماس به گرافیت ، با علم شیمی فیزیک توجیه میشود.
کاربردهای شیمی فیزیک
ارتباط شیمی فیزیک با سایر علوم ، کاربردهای اقتصادی و اجتماعی این علم را بیان میکند. به عنوان مثال ، با مطالعه الکتروشیمی ، به پایه و اساس پدیدههای طبیعی مانند خوردگی فلزات پی برده و میتوان از ضررهای اقتصادی و اجتماعی چنین پدیدههایی جلوگیری کرده و یا این پدیدهها را به مسیری مفید برای جامعه سوق داد. علاوه بر آن ، کاربرد قوانین ترمودینامیک مانند "نقطه اتکیتک" در جلوگیری از ضررهای جانی و مالی پدیدههای طبیعی مانند یخ بندان بعد از بارش برف ، بسیار مفید میباشد (مخلوط کردن برف و نمک بر اساس نقطه اتکیتک).
فراموش نکنیم که تمامی باطریها و پیلهایی که وسایل زندگی ما با نیروی آنها بکار گرفته میشوند، براساس قوانین شیمی فیزیک ساخته شدهاند.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 344 تاريخ : چهارشنبه 20 بهمن 1389 ساعت: 17:48
پژوهشگران توانستهاند دو حالت از آب مایع را مشاهده کنند که تا پیش از این تصور میشد فقط در دماهای پایینتر از دمای انجماد وجود دارد.

آب بدون شک عجیبترین مایع روی زمین است. برخلاف اکثر مایعات دیگر، هنگامی که منجمد میشود، چگالی آن کمتر میشود و جالب اینجاست که بیشترین چگالی آن نیز در پایینترین دمای آن به دست نمیآید؛ بلکه در 4 درجه بالای صفر به چگالی بیشینه خود میرسد. اینها فقط دو نمونه از خواص غیر عادی و پرشمار آب هستند که تعدادی از آنها برای عملکرد آن در محیط طبیعی خیلی مهم و حیاتی است. برای مثال چون یخ روی آب شناور میماند، دریاچهها در زمستان از پایین به بالا یخ نمیزنند.
پژوهشگران توانستهاند دو حالت از آب مایع را مشاهده کنند که تا پیش از این تصور میشد فقط در دماهای پایینتر از دمای انجماد وجود دارد.

آب بدون شک عجیبترین مایع روی زمین است. برخلاف اکثر مایعات دیگر، هنگامی که منجمد میشود، چگالی آن کمتر میشود و جالب اینجاست که بیشترین چگالی آن نیز در پایینترین دمای آن به دست نمیآید؛ بلکه در 4 درجه بالای صفر به چگالی بیشینه خود میرسد. اینها فقط دو نمونه از خواص غیر عادی و پرشمار آب هستند که تعدادی از آنها برای عملکرد آن در محیط طبیعی خیلی مهم و حیاتی است. برای مثال چون یخ روی آب شناور میماند، دریاچهها در زمستان از پایین به بالا یخ نمیزنند.
این رفتار غیر عادی از پیوندهای شیمیایی ضعیف آب ناشی میشود که پیوند هیدروژنی خوانده میشود و مولکولهای آب را در حالت مایع کنار هم نگاه میدارد. در یخ، این پیوند مولکولها را با فاصلهای معادل "یک دست از هم" نگاه میدارند، و در نتیجه فضای زیادی بین آنها باقی میماند.
در سال 1992 / 1371، جین استانلی از دانشگاه بوستون ماساچوست و همکارانش، شبیهسازیهای کامپیوتری از آب انجام دادند که نشان اگر آب در دمای خیلی پایین و تحت فشار بالایی قرار گیرد، میداد این پیوند هیدروژنی احتمالا دو نوع متفاوت از مایع را تولید میکنند. در یک حالت، شبکهای نسبتا باز و پراکنده از مولکولهای آب تشکیل میشود که آب کمچگال (LDL) نامیده میشود و در حالت دیگر، مولکولهای آب فشردهتر میشوند تا جاییکه برخی از پیوندهای هیدروژنی شکسته میشوند و آب پرچگال (HDL) شکل میگیرد.
استانلی و همکارانش دریافتند که این دو حالت آب در یک "تبدیل فاز" به هم تبدیل میشوند، مانند تبدیل فاز آب / یخ که آب و یخ را در مایع معمولی آب از هم جدا میکند. از این منظر، ویژگیهای عجیبی مانند بیشینه چگالی در دمای 4 درجه سانتیگراد، بازتابی از رقابت بین آب پرچگال و آب کمچگال است که در دماهای بسیار پایینتر سبب تبدیل فاز میشوند.
اکنون دینو لپورینی از دانشگاه پیزا در ایتالیا و همکارانش در موسسه ملی علوم هند در بنگلور میگویند که توانستهاند این دو حالت آب را که گروه استانلی در سال 1371 پیش بینی کرده بود، ببینند.
این ادعا، کارشناسان را به دو دسته تقسیم کرده است. استانلی این کار را برجسته مینامد، ولی پابلو دیبندتی که از متخصصان فیزیک مایعات در دانشگاه پرینستون در نیوجرسی است، میگوید که هرچند نتایج جالبی بدست آمده، «قطعا آن دلیل محکمهپسندی که مدتها به دنبالش میگشتند، نیست! دلیلی که ثابت کند که آب دو حالت مایع دارد که در دما و فشار خاصی به هم تبدیل میشوند».
یخ، شاید یخ

بخشی از مشکل به این برمیگردد که بررسی تجربی این دو حالت مفروض مایع خیلی سخت است، چرا که آب پیش از اینکه به دمایی که در آن احتمالا این دو حالت وجود دارند برسد؛ تمایل به انجماد دارد؛ یعنی دمای پایینتر از منفی 75 درجه سانتیگراد. در سال 1998 / 1377 استانلی و همکارش اوزامو میشیما از انستیتوی ملی تحقیقات مواد غیر آلی در تسوکوبا در ژاپن، هنگامی که یخ را با فشردهکردن به مایع تبدیل میکردند، نشانه کوچکی از تبدیل مایع به مایع را دیدند.
سپس در سال 2007 / 1386، فرانچسکو مالاماچی از دانشگاه مسینا در ایتالیا و همکارانش نشانههایی از دو نوع آب بسیار سرد محدودشده در منافذ سیلیکا را گزارش دادند که به حدی ریز بودند که به آب اجازه یخ زدن نمیدادند. البته این یافتهها، با این نقد مواجه شد که رفتار آب ممکن است به دلیل وجود منافذ بسیار ریز سیلیکا تغییر کرده باشد.
اما لپورینی و همکارانش فکر میکنند که توانستهاند این مشکل را با محدود کردن آب در خود یخ حل کنند. آنها از تکنیکی به نام رزونانس اسپین الکترون برای بررسی حرکت مولکولهای آب در محفظههای کوچک مایع که بین بلورهای یخ در دمای کمتر از منفی 183 درجه گیر افتادهاند، استفاده کردند.
پژوهشگران مستقیما حرکت آب را اندازه نگرفتند: در عوض، آنها حرکتهای یک مولکول آلی به نام تمپول را بررسی کردند که اگر گرانروی آب بیشتر شود، آهستهتر حرکت میکند. به گفته لپورینی این روش آنها را قادر میسازد که فقط حرکات آب محصور درون یخ را بررسی کنند، چرا که تمپول وارد یخ نمیشود.
آنها گزارش دادهاند که بین دمای منفی 140 و صفر درجه سانتیگراد، میتوانند دو نوع از حرکات تمپول را مشاهده کنند که احتمالا ناشی از حضور دو نوع از آب درون محفظههای یخی است. یکی از دیگری آهستهتر است و آنها این را به منزله حضور دو نوع مجزای آب تعبیر کردند: حالت LDL با گرانروی بیشتر و حالت سیالتر HDL است.
زندگی زیر یخ

دیبندتی قبول دارد که این نتایج، دلالت بر وجود دو نوع متفاوت از آب دارند که مقادیر نسبی آنها با تغییر دما تغییر میکند. ولی به نظر او هنوز شواهدی از این که این دو حالت آب، فازهای مشخص و مجزای آب باشند وجود ندارد. به گفته او ممکن است که آنها به تدریج به هم تبدیل شوند و هنوز معلوم نیست که تغییر مطلق حالت از یکی به دیگری وجود داشته باشد.
آوستین انجل، متخصص آب از دانشگاه ایالتی آریزونا در تمپا، حتی از این هم بدبینتر است. او فکر میکند همانطور که آب دریا هنگامی که یخ میزند نمک را از خود خارج میکند، این رگههای کوچک درون بلور یخ ممکن است شامل هر گونه ناخالصی باشند: «مایعی که نویسندگان مقاله بررسی کردهاند، آب خالص نیست؛ خوب وقتی که قسمت اعظم آب به بلور یخ تبدیل شده، چه چیزی باقی میماند؟ ترکیب آن مشخص نیست. حدس من این است آنچه مورد مطالعه قرار گرفته، ترکیب غلیظی از تمپول و ناخالصیهای محلول در آب بوده است».
در نتیجه قبل از این که بتوان نتایج را تایید کرد، باید کارهای زیادی انجام داد. ولی این مسلم است که حتی اگر این حق با منتقدین این تحقیقات باشد، باید دلیلی برای این ویژگیها وجود داشته باشد و علاوه بر آن خود این تحقیقات نیز راه را به دنیاهای جدیدی باز خواهد کرد. یکی از آنها میتواند احتمال وجود حیات در درون این کیسههای آب محصور درون یخ در قطبین و یا حتی در ذخایر یخ دیگر سیارات باشد، حیاتی که احتمالا وابسته به این دو نوع متفاوت آب خواهد بود.
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 261 تاريخ : پنجشنبه 12 فروردين 1389 ساعت: 3:39
دانشمندان دانشگاه توسان در بالتیمور با استفاده از یک عدسی ساده و صفحهای شیشهای، موفق شدند رنگینکمان را به دام بیاندازند و به یکی از آرزوهای دیرین انسان جامه عمل بپوشانند.
این تکنیک جدید که توسط ورا اسمولیانوا و همکارانش ابداع شده، ذخیره و نقل و انتقال اطلاعات را از طریق نور سادهتر خواهد کرد و شرایط را برای استفاده حداکثری از محاسبات و ارتباطات نوری فراهم خواهد نمود. فناوری نوری از فناوریهای رایج فعلی در علوم ارتباطات رایانهای و شبکه سریعتر است، اما دشواری فرآیند تبدیل نور به جریان الکتریکی و بالعکس، مهمترین ویژگی منفی آن است.

دانشمندان دانشگاه توسان در بالتیمور با استفاده از یک عدسی ساده و صفحهای شیشهای، موفق شدند رنگینکمان را به دام بیاندازند و به یکی از آرزوهای دیرین انسان جامه عمل بپوشانند.
این تکنیک جدید که توسط ورا اسمولیانوا و همکارانش ابداع شده، ذخیره و نقل و انتقال اطلاعات را از طریق نور سادهتر خواهد کرد و شرایط را برای استفاده حداکثری از محاسبات و ارتباطات نوری فراهم خواهد نمود. فناوری نوری از فناوریهای رایج فعلی در علوم ارتباطات رایانهای و شبکه سریعتر است، اما دشواری فرآیند تبدیل نور به جریان الکتریکی و بالعکس، مهمترین ویژگی منفی آن است.

در سال 2007 / 1386، اورتوین هس از دانشگاه ساری در انگلستان و همکارانش پیشنهاد دادند که پرتوهای نور را درون یک موجبر مخروطی بهدام بیاندازند. این موجبرها، ساختارهایی هستند که پرتوهای نور را در امتداد طول خود منتقل میکنند. برای ساخت این موجبر از متامتریال استفاده شده، موادی متشکل از مدارهای الکترونیکی که میتواند پرتوهای نور را با شیبهای تند منحرف کند.
ایده اصلی کار، این است که با باریکتر شدن موجبر ، پرتوهای نور نیز درمقابل مجبور شوند در نقاطی بسیار باریکتر متوقف شوند. این کار باتوجه به یکی از ابتداییترین اصول امواج قابل انجام است: هیچ موجی نمیتواند از حفرهای کوچکتر از نصف طولموجش عبور کند.
رنگینکمان چیست؟
رنگینکمان یکی از زیباترین پدیدههای جوی است که میتوان در روزهای بارانی منتظر آن بود. این پدیده هنگامی روی میدهد که پرتوهای سفیدرنگ خورشید در ارتفاع بالا به ریزقطرات کرویشکل باران برخورد میکنند و با تجزیه به طیفهای نور مریی (همان اتفاقی که در منشور روی میدهد) و بازتاب درون قطره، از آن خارج میشوند.
برای اینکه فردی بتواند رنگینکمان را ببیند، باید پشت به خورشید و رو به باران بایستد تا پرتوهای تجزیهشده و بازگشتی رنگینکمان را ببیند. در این حالت، فرد پرتوهایی در شش رنگ بنفش، آبی، سبز، زرد، نارنجی و قرمز را میبیند که با تقارن کروی به چشم او میرسند. چشم با امتداد دادن این پرتوها، کمانهایی شش رنگ را در آسمان تداعی میکند که همان رنگینکمان است.
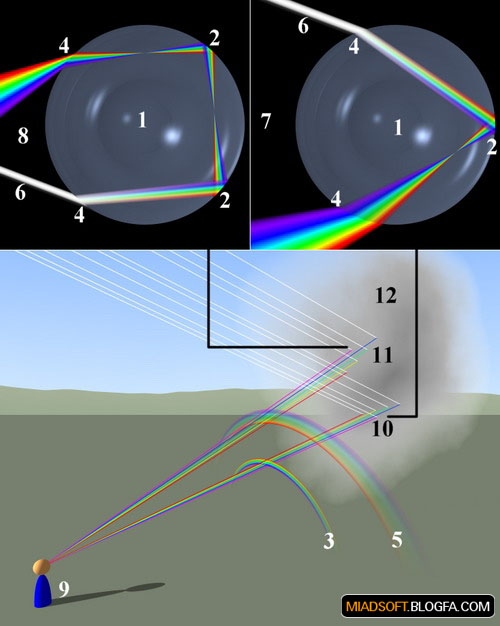
البته معروف است که رنگینکمان 7 رنگ دارد، درحالیکه این، اشتباهی تاریخی است. وقتی آیزاک نیوتن برای نخستین بار، پرتوهای خورشید را از درون منشور عبور داد و طیف تجزیهشده نور را بدست آورد، همین شش رنگ را دید؛ اما از آنجاکه در آن روزگار 7 عدد مقدسی بود، ترجیح داد رنگ نیلی را بین بنفش و آبی قرار دهد و با هفت رنگ ساختن طیف نور، توجه عمومی بیشتری را متوجه این پدیده سازد!
رنگینکمان وجود خارجی ندارد؛ یعنی شما نمیتوانید رنگینکمانی را بگیرید، یا پردهای برای نمایش آن برپا کنید، یا در محل آن فیلم عکاسی قرار دهید و اثرش را روی فیلم ثبت کنید. هر قدر تلاش کنید به رنگین کمان نزدیک شوید، رنگینکمان نیز به همان اندازه از شما دورتر میشود و همیشه در فاصلهای ثابت از شما باقی میماند. به همین دلیل است که تاکنون کسی موفق نشده بود رنگینکمان را به دام بیاندازد.
و رنگینکمان بهدام افتاد
شبیهسازیهای عددی نشان داد که چنین ایدهای حداقل روی کاغذ جواب میدهد، اما انجام آن توسط متامتریالها به یک رویا تبدیل شده بود. اما از قرار معلوم، ورا اسمولیانوا از دانشگاه توسان در مریلند بالتیمور و همکارانش توانستهاند با استفاده از یک عدسی محدب، توانستهاند این موجبر مخروطی را بسازند و رنگینکمانی از نور را بهدام بیاندازند.
آنها یکی از سطوح عدسی 4.5 میلیمتری خود را با لایهای 30 نانومتری از طلا پوشاندند و عدسی را از سطح طلادارش روی یک سطح شیشهای صاف که آننیز با لایهای از طلا پوشانده شده بود، قرار دادند. بدین ترتیب، فضای بین عدسی و سطح شیشهای، لایهای از هوا بود که ضخامت آن در لبهها (جایی که لبه دو عدسی روی هم قرار میگرفت) به صفر میرسید و میتوانست کار موجبر مخروطی را انجام دهد.
وقتی لیزر چندطیفی را از انتهای باز این مجموعه به داخل تاباندند، منظره جالبی به وقوع پیوست. اسمولیانوا با میکروسکوپ از بالا به عدسی نگاه کرد و مجموعهای از حلقههای رنگارنگ رنگینکمانی را درون آن دید، گویی رنگینکمانی داخل این قفس شیشهای به دام افتاده است.
اسمولیانوا این پدیده را چنین توضیح میدهد: «پرتوهای سبز که طولموج کوتاهتری دارند، در نقطهای به دام افتادند که موجبر بیش از اندازه برای عبور این پرتوها باریک شده بود. اما پرتوهای قرمز که طولموج بلندتری دارند، در فاصلهای دورتر به دام افتادند، جاییکه ضخامت موجبر بسیار بیشتر بود. پرتوهای زرد و نارنجی هم بین این دو به دام افتاده بودند، چراکه طولموج آنها بین این دو مقدار است».

برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 292 تاريخ : پنجشنبه 12 فروردين 1389 ساعت: 3:33
موج سرمای شدید در اروپا، این امکان را بهوجود آورده است که پدیدههای زیبایی را در هر خانهای تجربه کرد. یکی از این پدیدهها، حبابهای یخزده است که بلافاصله پس از متورم شدن، یخ میبندد.
یان راسل، مشاور نمایشگاههای علمی در شامگاه 6 ژانویه، این حبابهای آبصابون را در حیات منزلش تولید کرد. دمای هوا 6 درجه سانتیگراد زیر صفر بود و همین سبب شد حباب بهآرامی یخ بزند و او بتواند مراحل مختلف یخزدن را به تصویر بکشد.
اگر دمای هوا پایینتر از 20 درجه سانتیگراد زیر صفر میبود، حبابها بلافاصله یخ میبستند و کرههایی تشکیل میدادند که ضخامت آنها بیش از چند مولکول نبود. به بلورهای شش گوش یخ دقت کنید!





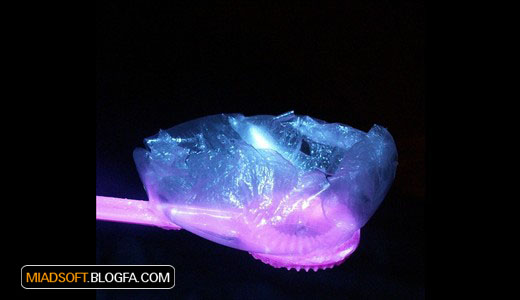
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 287 تاريخ : پنجشنبه 12 فروردين 1389 ساعت: 3:21
در حاشیه اجلاس سالانه شاخه دینامیک سیالات انجمن فیزیک آمریکا، نمایشگاهی از تصاویر حرکت سیالات و پدیدههای مرتبط با آن برگزار شد. گزارش تصویری امروز خبرآنلاین به مرور برترین این تصاویر میپردازد.

گردباد در انتهای بال هواپیما
اغلب در اطراف نوک بال هواپیماهای در حال پرواز، اشکالی شبیه به گردبادهای کوچک شکل میگیرند که میتوانند حرکت هواپیما را در ارتفاع پایین و نزدیک به زمین تحتالشعاع قرار دهند. این تصویر که به وسیله آشکارسازهای جریان گردبادی زمان برخورد با فلپهای چرخشی هواپیما تحت اثر نور لیزر به نمایش درآمده، پیچیدگی جریان حاصل را به وضوح نشان میدهد. علاوه بر جریان گردبادی اولیه که با رنگ قرمز نشانداده شده، جریان دومی هم وجود دارد که با رنگ سبز به نمایش درآمده و نتیجه برخورد بخشی از جریان گردبادی اولیه با زمین است.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 434 تاريخ : پنجشنبه 12 فروردين 1389 ساعت: 3:10
آب، فراوانترین مایع و بهجرات مهمترین مایعی است که روی زمین وجود دارد؛ اما اهمیت آن به پدیدههای زیستی منحصر نمیشود. ویژگیهای فیزیکی آب در مقایسه با دیگر مواد روی زمین، بینظیر است.
ما با معماهای زیادی مواجه هستیم، از طبیعت ماده تاریک و سر منشاء جهان گرفته، تا تحقیق برای نظریه همهچیز. اینها همه معماهایی در مقیاس بزرگ هستند، اما شما میتوانید معمای دیگری را از جهان فیزیکی مشاهده کنید که از آشپزخانه شما میآید (و اگر همانقدر بزرگ نباشد، به همان اندازه گیجکننده باشد). فقط یک لیوان را از آب سرد پر کنید، یک قالب یخ در آن بیاندازید و صبر کنید تا آب از تلاطم بیفتد.
این واقعیت که یخ شناور میشود، اولین مورد عجیب این ماده است. زمانی معما عمیقتر میشود که با استفاده از یک دماسنج دمای آب را در اعماق مختلف اندازه بگیرید. در بالا و در نزدیک قالب یخ، میبینید که دمای آب نزدیک به صفر درجه است، اما در انتهای لیوان دما به 4 درجه میرسد. دلیل آن این است که چگالی آب در دمای 4 درجه سلسیوس، از هر دمای دیگری بیشتر است (یک ویژگی عجیب دیگر که آن را از هر مایع دیگری متمایز میسازد).
خواص عجیب آب همچنان ادامه دارد و برخی از آنها برای زندگی حیاتی هستند. به دلیل اینکه چگالی یخ از آب کمتر است و چگالی آب در نقطه انجماد کمتر از زمانی است که آب تا چهار درجه گرمتر باشد، آب نسبت به ته لیوان، از بالا به پایین منجمد میشود. بنابراین حتی در طول عصر یخ بندان، زندگی در اعماق دریاها و اقیانوسها همچنان ادامه داشت. آب ظرفیت خارقالعادهای برای گرفتن گرما دارد و این به ملایمتر کردن تغییرات آبو هوایی کمک میکند، که در غیر این صورت میتواند اکوسیستمها را نابود کند.
با این حال، به رغم اهمیت بسیار زیاد آب برای حیات، هیچ نظریه واحدی دست کم تا کنون نتوانسته یک توضیح قابل قبول برای خصوصیات اسرارآمیز آن ارائه کند. اگر ما بتوانیم نظریات اندرس نیلسون از فیزیکدانان دانشگاه استنفورد کالیفرنیا، و لارس پترسون از دانشگاه استکهلم سوئد، و همکاران این دو را بپذیریم؛ بالاخره توانستهایم به دلیل واقعی خیلی از این خصوصیات غیر عادی پی ببریم.
نظریات جنجالی این دو، بسط دهنده نظریهای است که بیش از یک قرن پیش از این توسط ویلهلم رونتگن، کاشف اشعه ایکس، ارائه شده است. او ادعا کرده بود که مولکولها در آب مایع آن گونه که در کتابهای امروزی میبینیم، تنها از یک طریق به هم نپیوستهاند، بلکه این اتصال از دو مسیر کاملا متفاوت انجام میشود.
ساختار اسرارآمیز آب
کلید فهم اسرار آب، نحوه تعامل مولکولهای آن با همدیگر است، مولکولهایی که از یک اتم اکسیژن و دو اتم هیدروژن تشکیل شدهاند. اتم اکسیژن بار منفی ناچیزی دارد و اتمهای هیدروژن، در مجموع بار مثبتی معادل آن دارند. به همین ترتیب، اتمهای هیدروژن و اکسیژن مولکولهای همسایه، از طریق تشکیل پیوندی به نام پیوند هیدروژنی به همدیگر جذب میشوند.
پیوندهای هیدروژنی، خیلی ضعیفتر از پیوندهایی هستند که اتمها را در مولکولها در کنار هم قرار میدهند، و به همین دلیل همواره در حال گسیختن و بازپیوستن هستند. این پیوندها هنگامی به حداکثر قدرت خود میرسند که مولکولها به نحوی کنار هم قرار گرفته باشند که هر پیوند هیدوژنی در امتداد یک پویند مولکولی قرار بگیرد. شکل یک مولکول آب به نحوی است که هر مولکول H2O در میان چهار مولکول همسایه قرار میگیرد و یک هرم با قاعده مثلثی را تشکیل میدهد، که معمولا به نام تتراهدرون یا چهارسطحی شناخته میشود.
آب، فراوانترین مایع و بهجرات مهمترین مایعی است که روی زمین وجود دارد؛ اما اهمیت آن به پدیدههای زیستی منحصر نمیشود. ویژگیهای فیزیکی آب در مقایسه با دیگر مواد روی زمین، بینظیر است.
ما با معماهای زیادی مواجه هستیم، از طبیعت ماده تاریک و سر منشاء جهان گرفته، تا تحقیق برای نظریه همهچیز. اینها همه معماهایی در مقیاس بزرگ هستند، اما شما میتوانید معمای دیگری را از جهان فیزیکی مشاهده کنید که از آشپزخانه شما میآید (و اگر همانقدر بزرگ نباشد، به همان اندازه گیجکننده باشد). فقط یک لیوان را از آب سرد پر کنید، یک قالب یخ در آن بیاندازید و صبر کنید تا آب از تلاطم بیفتد.
این واقعیت که یخ شناور میشود، اولین مورد عجیب این ماده است. زمانی معما عمیقتر میشود که با استفاده از یک دماسنج دمای آب را در اعماق مختلف اندازه بگیرید. در بالا و در نزدیک قالب یخ، میبینید که دمای آب نزدیک به صفر درجه است، اما در انتهای لیوان دما به 4 درجه میرسد. دلیل آن این است که چگالی آب در دمای 4 درجه سلسیوس، از هر دمای دیگری بیشتر است (یک ویژگی عجیب دیگر که آن را از هر مایع دیگری متمایز میسازد).
خواص عجیب آب همچنان ادامه دارد و برخی از آنها برای زندگی حیاتی هستند. به دلیل اینکه چگالی یخ از آب کمتر است و چگالی آب در نقطه انجماد کمتر از زمانی است که آب تا چهار درجه گرمتر باشد، آب نسبت به ته لیوان، از بالا به پایین منجمد میشود. بنابراین حتی در طول عصر یخ بندان، زندگی در اعماق دریاها و اقیانوسها همچنان ادامه داشت. آب ظرفیت خارقالعادهای برای گرفتن گرما دارد و این به ملایمتر کردن تغییرات آبو هوایی کمک میکند، که در غیر این صورت میتواند اکوسیستمها را نابود کند.
با این حال، به رغم اهمیت بسیار زیاد آب برای حیات، هیچ نظریه واحدی دست کم تا کنون نتوانسته یک توضیح قابل قبول برای خصوصیات اسرارآمیز آن ارائه کند. اگر ما بتوانیم نظریات اندرس نیلسون از فیزیکدانان دانشگاه استنفورد کالیفرنیا، و لارس پترسون از دانشگاه استکهلم سوئد، و همکاران این دو را بپذیریم؛ بالاخره توانستهایم به دلیل واقعی خیلی از این خصوصیات غیر عادی پی ببریم.
نظریات جنجالی این دو، بسط دهنده نظریهای است که بیش از یک قرن پیش از این توسط ویلهلم رونتگن، کاشف اشعه ایکس، ارائه شده است. او ادعا کرده بود که مولکولها در آب مایع آن گونه که در کتابهای امروزی میبینیم، تنها از یک طریق به هم نپیوستهاند، بلکه این اتصال از دو مسیر کاملا متفاوت انجام میشود.
ساختار اسرارآمیز آب
کلید فهم اسرار آب، نحوه تعامل مولکولهای آن با همدیگر است، مولکولهایی که از یک اتم اکسیژن و دو اتم هیدروژن تشکیل شدهاند. اتم اکسیژن بار منفی ناچیزی دارد و اتمهای هیدروژن، در مجموع بار مثبتی معادل آن دارند. به همین ترتیب، اتمهای هیدروژن و اکسیژن مولکولهای همسایه، از طریق تشکیل پیوندی به نام پیوند هیدروژنی به همدیگر جذب میشوند.
پیوندهای هیدروژنی، خیلی ضعیفتر از پیوندهایی هستند که اتمها را در مولکولها در کنار هم قرار میدهند، و به همین دلیل همواره در حال گسیختن و بازپیوستن هستند. این پیوندها هنگامی به حداکثر قدرت خود میرسند که مولکولها به نحوی کنار هم قرار گرفته باشند که هر پیوند هیدوژنی در امتداد یک پویند مولکولی قرار بگیرد. شکل یک مولکول آب به نحوی است که هر مولکول H2O در میان چهار مولکول همسایه قرار میگیرد و یک هرم با قاعده مثلثی را تشکیل میدهد، که معمولا به نام تتراهدرون یا چهارسطحی شناخته میشود.
دست کم، این راهی است که مولکولها در یخ در کنار هم قرار میگیرند. از یک دیدگاه متعارف سنتی، آب مایع یک ساختار مشابه ولی کمتر صلب دارد، که در آن مولکولهای بیشتری میتوانند در برخی از فضاهای خالی در یک آرایش چهار سطحی قرار بگیرند. این امر توضیح میدهد که چرا آب مایع از یخ چگالتر است، و به نظر میرسد که با نتایج آزمایشهای گوناگون که در آنها پرتوهای ایکس، فرو سرخ و نوترونها، از نمونههای آب منعکس میشوند همخوانی داشته باشد.
برخی از فیزیکدانها ادعا کردهاند که آبی که تحت شرایط به خصوصی قرار گرفته باشد، به دو ساختار کاملا متفاوت تجزیه میشود. ولی اکثر آنها چنین فرض میکنند که در شرایط عادی، تنها یک ساختار وجود دارد.
اما ده سال قبل، یک کشف اتفاقی توسط پترسون و نیلسون، این تصویر را به چالش کشید. آنها در حال استفاده از طیفسنجی جذبی اشعه ایکس برای تحقیق در مورد آمینو اسید گلیسین بودند. نقاط پیک در طیف جذبی اشعه ایکس میتواند ماهیت دقیق اتصالات شیمیایی ماده هدف را مشخص کنند، و همچنین به تعیین ساختار آن کمک کنند. نکته مهم این بود که آن دو از یک منبع جدید قدرتمند اشعه ایکس استفاده میکردند که میتوانستند با استفاده از آن، اندازهگیریهای حساستر و دقیقتری را نسبت به آن چه تا پیش از این ممکن بود انجام دهند. آنها به زودی دریافتند که آبی که حاوی نمونه گلیسین بود، طیف خیلی جالبتری به نسبت خود آمینو اسید تولید میکرد. نیلسون میگوید: «آنچه ما دیدیم بسیار شورانگیز بود، بنابراین ما احساس کردیم که باید به کنه آن پی ببریم».
مفاهیم مهیج
ویژگی که توجه آنها را جلب کرد یک نقطه پیک در طیف جذبی بود که توسط مدلهای سنتی آب مایع پیشبینی نشده بود. در حقیقت، در مقالهای که آنها در سال 2004 منتشر کردند چنین نتیجه گرفتند که در هر لحظه، 85 درصد از پیوندهای هیدروژنی در آب، باید تضعیف و یا شکسته شده باشند. این مقدار خیلی بیشتر از 10 درصدی است که توسط مدلهای کتب درسی پیشبینی شده است.
مفاهیم این یافته بسیار جالب توجه هستند: این به معنی آن است که یک بازنگری کامل در ساختار آب مورد نیاز است. در نتیجه نیلسون و پترسون شروع به انجام آزمایشهای دیگری با پرتو ایکس برای اثبات ادعای خود کردند. اولین حرکت آنها استقبال از کمک شیک شین از دانشگاه توکیو در ژاپن بود. وی متخصص تکنیکی است که «طیفسنجی نشری اشعه ایکس» نام دارد. نکته کلیدی در مورد این طیفسنجی این است که در طیف نشری یک ماده، هر چه طولموج اشعه ایکس کوتاهتر باشد، پیوند هیدروژنی باید ضعیفتر باشد.
نتیجه عالی بود: طیف اشعه ایکس نشری، شامل دو نقطه پیک بود که ممکن بود ناشی از دو ساختار جداگانه باشند. اعضای گروه چنین استدلال کردند که پیک مربوط به اشعههای ایکس با طولموج بلندتر، نشان دهنده سهم مولکولهایی است که به صورت چهار سطحی آرایش یافتهاند، در حالی که پیک طولموج کوتاهتر، بازتاب دهنده سهم مولکولهایی است که ساختار متفاوتی دارند.
جالب اینجا بود که پیک طولموج کوتاهتر در نشر اشعه ایکس شدیدتر از دیگری بود. این بدان معنی است که مولکولهای با پیوند ضعیفتر در آن نمونه، شایعتر بودند؛ و این خود تاییدی بر ادعای پیشین اعضای گروه بود. علاوه بر آن، آنها همچنین دریافتند که هر چه آب گرمتر باشد، این پیک به طولموجهای کوتاهتری منتقل میشود؛ در حالی که پیک دیگر، کمابیش ثابت باقی میماند.
این بدان معنی است که پیوندهای هیدروژنی اتصال دهنده مولکولهای موجود در این ساختار متفاوت، در اثر گرما بیشتر تضعیف میشوند؛ که باز هم با پیشبینیهای گروه مطابقت داشت. آنها سپس دادههای تجربی قدیمیتر را، که به نظر میرسید که با شکل سنتی آب مطابقت دارد، دوباره بررسی کردند و اکنون ادعا میکنند که این نتایج نیز با مدل جدید مطابقت دارد.
اگر آنها درست بگویند سوال دیگری مطرح میشود: تفاوتها در ساختارهای مختلف در مایع تا چه اندازه است؟ برای یافتن پاسخ، آنها از یک اشعه ایکس پرتوان استفاده کردند که در منبع نور تابشی سینکرترون دانشگاه استنفورد در کالیفرنیا تولید شده بود. این بار، چگونگی پراکندن پرتوهای ورودی از زاویههای مختلف به سطح آب، مورد ارزیابی واقع شدند. به گفته آنها، نتایج آشکار میکند که آب پوشیده از نواحی کوچکی از مولکولهایی است که به صورت چهار سطحی آرایش یافتهاند، و هر طول هر ناحیه نیز بین 1 تا 2 نانومتر است..
با ترکیب ای یافتهها با اندازهگیریهای دیگری که توسط اووه برگمن در دانشگاه استانفورد انجام شدهبود، آنها نتیجه گرفتند که ساختارهای منظم، که هر یک به طور متوسط شامل50 تا 100 مولکول هستند، توسط دریایی از پیوندهای مولکولی ضعیف احاطه شدهاند. ولی این نواحی ثابت نیستند. در کمتر از یک تریلیونیوم ثانیه، مولکولهای آب بین دو حالت گسست و باز تولید پیوندهای هیدروژنی نوسان میکنند.
توضیح غیر قابل توضیح!
توازن متغیر بین دو نوع آب که توسط نیلسون و پترسون مطرح شده بود، میتواند توضیحی باشد بر اینکه چرا آب در دمای 4 درجه به بیشترین چگالی خود میرسد. در نواحی آشفته مولکولهای آب به هم نزدیکتر هستند که این خود باعث چگالتر شدن آب نسبت به نواحی میشود که مولکولهای آب در ساختار چهار سطحی منظم آرایش داده شدهاند. در دمای صفر درجه نواحی آشفته نسبتا کمیاب هستند اما زمانی که آب گرمتر میشود، انرژی گرمایی اضافی تمایل بیشتری به لرزاندن و جدا کردن ساختارهای منظمتر مییابد. بنابراین مولکولها زمان کمتری را در ساختارهای منظم چهار سطحی و مدت زمان بیشتری را در نواحی آشفته سپری میکنند، امری که در مجموع باعث بیشتر شدن چگالی میشود.
از سوی دیگر، زمانیکه دما افزایش مییابد، حرکت مولکولهای با پیوند ضعیفتر بیشتر خواهد شد و همین مسئله بهتدریج آنها را وا میدارد که از هم دورتر شوند. این بسط که یک بار به توضیح دلیل چگالی بیشینه آب در دمای چهار درجه سلسیوس بالای صفر کمک کرده بود، این بار نیز به توضیح دلیل کاهش چگالی و افزایش حجم آب با افزایش بیشتر دمای آن کمک میکند.
به عقیده پترسون، این نظریه توضیحات کاملی را برای بسیاری از خواص غیرطبیعی غیر قابل توجیه دیگر آب ارائه میکند. مواردی که به ادعای آن دو، دیگر نظریهها هنوز نتوانستهاند به آن دست یابند. مارتین چاپلین، که یک شیمیدان در دانشگاه ساوث بنک لندن است، با این نظریه موافق است. توضیحاتی که بر مبنای سیستم تک مولفهای متعارف بودند، مجبور بودند زمانی که دمای آب تغییر میکند تلاش زیادی بکنند تا بتوانند ویژگیهای متعدد آب از قبیل کمینه و بیشینه را با نظریه خود سازگار کنند. چاپلین میگوید: «ساختار دوگانه کاملا با آزمایشها همخوانی دارد و میتواند خصوصیات غیر عادی آب را خیلی سادهتر از مدلهای سنتی توضیح دهد».
به مقاله سال 2004 نیلسون و پترسون در مجله ساینس تا کنون بیش از 350 بار و توسط محققین دیگر، ارجاع شده است. با این حال، هنوز خیلیها بدبین هستند. یک بدبینی این است که توضیح گروه در مورد نتایج طیفسنجی اشعه ایکس، بر مبنای شبیه سازی دست کم 50 مولکول آب در حال تعامل با هم است. یک مدل بینهایت پیچیده که تنها میتواند به طور تقریبی حل شود. ریچارد سایکالی از دانشگاه برکلی کالیفرنیا میگوید: «ما نیاز به یک نظریه خیلی دقیقتر داریم تا بتوانیم چنین ادعای بزرگی را بپذیریم». او ادعا میکند که تنظیمات کوچک برای آرایش پیوندهای هیدروژنی در ساختارهای متعارف، برای توضیح نتایج اشعه ایکس پترسون و نیلسون کفایت میکنند. حتی یکی از اعضای گروه آنها، مایکل اوبلیوس از دانشگاه استکهلم، همکاری خود را با آنها قطع کرد چرا که با تفسیر آنها از دادههای نشر اشعه ایکس موافق نبود.
یک نکته جزئی که خیلی از افراد را به این نظریه بدبین کرده بود، یک ادعا در مقاله سال 2004 بود که مولکولهایی که پیوند ضعیفتری دارند، تشکیل حلقه و زنجیره میدهند؛ و در واقع نیلسون و همکارانش نیز اکنون کمتر در مورد جزئیات ساختار مولکولی نامنظم اظهار نظر میکنند. ولی یوجین استنلی ازدانشگاه بوستون، باور ندارد که این امر کاملا نظریه آنها را زیر سوال میبرد: وی میگوید: «من فکر نمیکنم که آنها باید تا ابد محکوم شوند». به رغم این که نظریه آنها هنوز جای کار دارد، ولی به گفته او، نتایج پراکنش اشعه ایکس شواهدی بر تایید نظریه آنها ارائه میکند.
هیچ شکی نیست که هنوز نیلسون و پترسون با مخالفتهای شدیدی مواجه خواهند بود، ولی پاداشهای یک درک فراگیر از ساختار آب مایع میتواند شایان توجه باشد. این درک میتواند منجر به درک بهتر از مواردی مانند چگونگی برهمکنش پروتئینها و داروها با مولکولهای آب در بدن، و در نتیجه تولید داروهای موثرتری گردد. با دادن یک ایده بهتر از چگونگی رفتار مولکولهای آب در اطراف منافذ ریز ما، میتواند به تلاشها برای نمک زدایی و تصفیه آب کمک کند و سطح دسترسی به آب تمیز را بیشتر کند.
پترسون میگوید: «درک ما از آب یک تصویر در حال تکامل است. پیش از تکمیل این تصویر، تحقیقات بیشتری باید توسط گروههای مختلف انجام شود». چه کسی میتواند با این حرف مخالفت کند؟
سایت رشته صنایع شیمیایی...برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 269 تاريخ : پنجشنبه 12 فروردين 1389 ساعت: 2:42
رنگ يك ماده مهندسي ميباشد، اما برخلاف بعضي از مواد مهندسي يك ماده ساده نيست، يا حتي نمي توان آن را به سادگي به صورت دسته اي از مواد تعريف كرد. رنگ مي تواند از هزاران ماده شيميايي طبيعي و مصنوعي آلي و معدني تشكيل شود. تهيه فيلمهائي از رنگ كه تاثيرات مطلوب را به همراه داشته باشند مستلزم به كارگيري استادانه انواع بسياري از تكنيكهاي مهم با استفاده از مواد اوليه مي باشد.
بدون شك هرگاه شخصي مواد خامي را كه امروزه تهيه كنندگان پوششهاي آلي مورد استفاده قرار مي دهند با مواد مصرفي 40 سال قبل مقايسه كند از افزايش تعداد و انواع آنها متحير خواهد شد. در حقيقت تعداد بي شماري رزين مصنوعي، روغن و رقيق كننده با انواع وسيعي از رنگدانه هاي معدني و آلي وجود دارند كه مي توان در ساخت يك پوشش آلي از آنها استفاده كرد. بنابراين، مي توان گفت كه ساده ترين پوشش ساخته شده در حقيقت يك سيستم پيچيده است.
يك رنگ براي مصرف كننده نهائي بايد داراي خصوصياتي از قبيل سهولت استعمال، خشك شدن سريع و عدم سينه دادن، ته نشين شدن، جداشدن رنگدانه ها، ژل شدن، پوسته زدن و در نهايت پايداري هنگام نگهداري را دارا باشد. افزودن مقدار كمي از تركيباتي به غير از تركيبات معمولي و اصلي رنگ، براي دستيابي به خواص عملي مطلوب، به دورانهاي اوليه صنعت برميگردد. در طول دوران صنعت تاكنون تركيباتي از قبيل صابونها، چسبها،سفيده تخم مرغ، صمغهاي طبيعي و نوعي از آسفالت به نام گيلسونت همواره براي اين منظور مورد استفاده قرار مي گرفته است. امروزه، با وجود اين كه هنوز تعدادي از اين مواد مورد استفاده قرار مي گيرند، اما مصرف مواد اضافه شونده مصنوعي رو به افزايش نهاده است. در يك عبارت كلي، هر يك از اجزاي سازنده رنگ، در حقيقت، يك ماده اضافه شونده است. سازنده هاي رنگ به دو دسته تقسيم مي شوند: قسمت اول شامل آن دسته از مواد ميباشد كه براي يك رنگ اساسي هستند و قسمت دوم شامل موادي كه به منظور بهبود و اصلاح طبيعت و كيفيت رنگ، سهولت روشهاي استعمال آن، يا بعضي هدفهاي ديگر مورد استفاده قرار مي گيرند.
يك رنگ متشكل از رنگدانه، رزين، حلال، خشك كن يا ماده سخت كننده ميباشد. با وجود اين، هيچ لزومي ندارد كه همواره تمام اين مواد در يك رنگ وجود داشته باشند. برعكس در اغلب رنگها، مواد اوليه فوق براي به وجود آوردن يك ماده پوشش دهنده نهائي به تنهائي كافي به نظر نمي رسند. اما به هر حال اين مواد جزء مواد اصلي رنگ به شمار مي روند.
يك فرمول كننده رنگ مي تواند از مواد اضافه شونده به عنوان ابزار اساسي براي اصلاح و بهبود پوششها استفاده كند. در صورت استفاده صحيح از مواد اضافه شونده فرمول كننده رنگ مي تواند، بدون هيچگونه افزايش در قيمت رنگ، و يا حتي با كاهش دادن آن بدون كاهش كيفيت، رنگي با بالاترين كيفيت را توليد نمايد. بنابراين، مواد اضافه شونده يك جزء لازم از پوششها را تشكيل مي دهند.
مواد اضافه شونده در رنگ ها
انواع مواد اضافه شونده به رنگ ها که استفاده قرار مي گيرند، عبارتند از:خشک کن ها ، مواد ضد پوسته، مواد تعديل كننده گرانروي و مواد ضد رسوب، ضد سينه دادن، مواد پخش كننده، موادي كه كمك به همتراز شدن سطح فيلم رنگ مي كنند ، مواد بازدارنده خوردگي ، مواد ضد كپك يا باكتري ، مواد ضد خزه يا ضد جلبك ، موتد ضد كف يا كف زدا ، مواد ضد يخ ، مواد جاذب نور فرابنفش ، مواد كند كننده آتش سوزي ، مواد خوشبو كننده و بو زدا ، مواد مقاوم كننده فيلم رنگ در مقابل رطوبت ، موادي كه باعث افزايش نقش چكشي رنگهاي چكشي مي شوند ، مواد كنترل كننده برق فيلم رنگ (مواد مات كننده) و مواد نرم كننده.
خشك كنها:
به طور كلي زماني كه فيلم يك رنگ خشك مي شود مراحل زير اتفاق مي افتد:
1- تبخير مواد فرار: اين عمل به ترتيب باعث مي شود كه :
مايع رنگ غليظ شود؛
جدائي فاز صورت گيرد(ژلاتيني شدن يا بلور شدن)؛
فشارهاي حاصل از انقباض فيلم موجب فشرده شدن دانسيته فيلم گردد؛
رنگ بر روي شيء پخش گردد و آن را مرطوب سازد تا سطح چسبنده اي بين شيء و رنگ ايجاد شود؛
پوسته فيلم كشيده شده و مولكولهائي كه در سطح تماس با هوا واقعند دوباره سازمان دهي شوند؛
رنگدانه ها ته نشين و يا غوطه ور شوند.
2- جذب اكسيژن و ساير گازها از هوا: در بسياري از موارد در خلال جذب اكسيژن واكنشهائي صورت مي گيرد كه باعث مي شود تعداد نسبتا كمي از مولكولها به منومترهاي قابل پليمر شدن تبديل گردند.
3- مولكولهاي كوچكتر مولكولهاي بزرگتر را تشكيل مي دهند، و در اين ميان واكنشهاي حلقوي صورت مي گيرد.
4- ممكن است جدائي فاز صورت گيرد: كه در آن مولكولهاي پيچيده نامحلول به صورت ذرات امولسيوني كوچك(يا ميكرو ژلها) جدا شده و به شكل كلوئيدي در فاز مايع معلق مي شوند. مايع پيوستگي خود را به عنوان يك محيط معلق كننده براي كلوئيد حفظ مي كند، زيرا هنوز مولكولهائي از ذرات همنوع و غير همنوع وجود دارند كه از نظر مولكولي در يك مخلوط بي نظم قابل مخلوط كردن با يكديگر ميباشند تا يك مايع بي شكل را بوجود آورند.
5- ژلاتيني شدن: كه نمايانگر آخرين مرحله خشك شدن فيلم رنگ مي باشد و آن را مرحله دگرگوني فاز نيز مي نامند. در اين مرحله ذرات پراكنده يك شبكه به هم پيوسته را تشكيل مي دهند، و به اين ترتيب جامد خلل و فرج داري بوجود مي آيد كه در حقيقت بخشي از فيلم خشك شده رنگ ميباشد، و مايع باقيمانده در درون فضاهاي خالي اين جامد جاي مي گيرد. گاهي اوقات قبل از اينكه تمام حلال تبخير شده باشد ژلاتيني شدن اتفاق مي افتد يا ممكن است اين عمل تا زماني كه بخش اعظمي از حلال تبخير و اكسيداسيون بيشتري انجام شود صورت نگيرد.
در بعضي از انواع پوششهاي آلي براي تسريع خشك شدن فيلم رنگ از موادي استفاده مي شود كه آنها را خشك كن مي نامند. خشك كنها را مي توان به عنوان كاتاليزورهائي تعريف كرد كه وقتي به رنگ افزوده مي شوند باعث تسريع در خشك شدن يا سخت شدن فيلم رنگ مي گردند. بضي ها خشك كنها را به عنوان«قاصداني» تعريف كرده اند كه مولكولهاي اكسيژن هوا را مي ربايند و آنها را به مولكولهاي روغن خشك شونده يا نيمه خشك شونده به كار رفته در ساختمان مولكولي رنگپايه رنگ مي رسانند و همين مراحل دوباره تكرار مي شود تا اكسيژن بيشتري به مولكولهاي روغن برسد.
ضد پوسته ها:
زماني يك فيلم قابل استفاده و عرضه به بازار خواهد بود كه بتواند حداقل فيلمي با شرايط مورد نظر تشكيل داده و در زمان مناسب خشك شود. براي ارائه فرمول يك رنگ زمان، انرژي و تلاش بسياري صرف مي شود تا با تعيين نوع و مقدار صحيح از يك يا چند خشك كننده رنگي با بهترين خواص خشك شوندگي تهيه شود. منظور از بهترين خواص خشك شوندگي در يك رنگ آن است كه در هنگام استعمال رنگ بر روي سطح پس از آنكه به صورت فيلم درآمد در زمان مناسب همراه با ايجاد بهترين خصوصيات فيزيكي خشك شود. بنابراين، هرگاه رنگ در زمان و مكاني به غير از زمان و مكان استعمال آن خشك شود، مورد قبول نخوهد بود و اين همان پوسته بستن رنگ، از جمله عيوب مهم آن ميباشد.
به طور كلي، پوسته بستن رنگ مربوط به تمايل پليمر شدن و اكسايش رنگپايه هاي مصرفي در پوششهاي محافظت كننده ميباشد كه موجب خشك شدن رنگ مي گردد. ما مي خواهيم كه رنگ پس از استعمال بر روي سطح خشك شود. و به همين منظور به آن خشك كن اضافه مي كنيم. در بعضي فرمول بنديها نه تنها از اين طريق به خشك شدن كلي فيلم رنگ دست مي يابيم، بلكه يك خشك شدن سطحي سريع نيز در رنگ ايجاد مي شود كه موجب تشكيل يك پوسته نازك بر روي سطح رنگ مي گردد. اگر بخواهيم براي جلوگيري از پوسته بستن مقدار خشك كن را كم كنيم، تنها زمان خشك شدن را افزايش داده ايم نه اينكه از پوسته بستن جلوگيري كرده باشيم. اين مسئله مخصوصا در پوششهاي سريع خشك شونده آشكار ميباشد. البته لازم به تذكر است كه مسئله پوسته بستن رنگ هميشه جزء عيوب رنگ نيست، بلكه در بعضي رنگهاي تجارتي كه بايد پس از خشك شدن، فيلم آنها چين و چروك دار باشد مسئله پوسته بستن از اهميت به سزائي برخوردار خواهد بود.
مي توان گفت كه طبيعت اجزاي متشكله يك رنگ در كارآئي آن، از جمله پوسته بستن، از اهميت خاصي برخوردار است. همچنين علاوه بر طبيعت اجزاي متشكله رنگ، ميزان هر يك از آنها نيز در پيدايش خصوصيات مثبت و منفي رنگ موثر هستند. براي مثال، وقتي كه در يك رنگ ميزان خشك كنهاي مصرفي بيش از حد معمول باشد، موجب شدت پوسته بستن رنگ مي گردد. از طرف ديگر وجود حلالهاي شديدا فرار رنگي كه درب قوطي آن محكم بسته شده و كاملا به دور از هوا ميباشد، امكان تشكيل پوسته را به حداقل كاهش ميدهد. البته هرگونه كاهشي در گرانروي سيستم رنگ نيز موجب كاهش تمايل به پوسته بستن مي گردد، همانطوريكه هرگونه كاهشي در درصد مواد جامد رنگپايه نيز اين كار را انجام ميدهد.
از ميان عواملي كه موجب پوسته بستن رنگ مي گردند مي توان به موارد زير اشاره كرد:
1- اكسايش سطح رنگ در ظرف محتوي آن؛
2- ژل شدن رنگ در اثر كاهش حلال؛
3- تركيبي از دو مورد 1 و 2 كه موجب به هم خوردن موازنه كلوئيدي رنگ مي گردد.
بهترين راه براي جلوگيري از پوسته بستن افزودن مواد ضد اكسايش به رنگ ميباشد. اين گونه مواد بدون آنكه اثر سوئي بر روي خواص مطلوب رنگ داشته باشند، اثرات زيان بار اكسايش زود هنگام رنگ را خنثي مي سازند. بسياري از چربيها و روغنهاي چرب به طور طبيعي حاوي مواد ضد اكسايش مي باشند و در نتيجه از نظر پوسته بستن مسئله اي را ايجاد نمي كنند. اما در موادي كه مقدار اين مواد در حد كافي نباشد بايد از مواد افزودني ديگر استفاده كرد.
در ارزيابي و انتخاب يك ماده ضد پوسته علاوه بر چگونگي عملكرد آن در جلوگيري از پوسته بستن، چندين عامل ديگر نيز در نظر گرفته مي شود كه عبارتند از:
1- ميزان تاثير آن در كند كردن زمان خشك شدن؛
2- سازگاري با سيستمهاي رنگ و جلا؛
3- ميزان تاثير آن در تغيير رنگ يا بد رنگ كردن فيلم خشك شده؛
4- ميزان تاثير آن در تغيير رنگ يا بد رنگ كردن اجزاي مايع جلا؛
5- بو.
علاوه بر اين ، يك ماده ضد پوسته نبايد هيچ گونه اثر زيان آوري بر روي گرانروي يا ساير خواص رئولوژيكي رنگ، چه در ابتدا و چه در خلال زمان انبار كردن،داشته باشد. همچنين، ماده ضد پوسته نبايد اثر ناخواسته و نامطلوبي بر روي براقيت و دوام كلي فيلم رنگ بگذارد.
كارآئي ضد پوسته هاي مختلف با نوع رنگپايه اي كه ضد پوسته در آن مورد استفاده قرار مي گيرد، فرق مي كند. مواد ضد پوسته را مي توان به سه دسته تقسيم كرد :
1- اكسيم ها
2- پلي هيدروكسي فنلها و مشتقاتش
3- موادي از نوع حلالها كه به عنوان يك ماده ديسپرس كننده محصولات شديدا پليمري عمل كرده و در نتيجه مانع ژل شدن ذرات مي گردند.
مواد تعديل كننده گرانروي و مواد ضد رسوب :
فرمول بندي رنگ ممكن است موجب توليد رنگهائي شود كه بيش از حد سيال و روان باشند. رنگ مايعي كه گرانروي آن پائين باشد ممكن است سياليت آن بيش از حد لزوم براي مقصود نهائي باشد، هر چند سياليت زياد در شرايط ممكن است بسيار سودمند هم باشد. بنابراين گرانروي پائين در رنگين كننده ها، بتونه ها و لاكهاي اسپري ممكن است مطلوب باشد ولي در پوششهائي كه فيلم خشك شده آنها ضخامت بالائي دارد و همچنين رنگهائي كه به وسيله قلم مو مصرف مي شوند، چنين نمي باشند. در رنگهاي با گرانروي پائين، رسوب رنگدانه ها در خلال مدت نگهداري، بخصوص اگر رنگدانه ها بهم فشرده باشند،اتفاق مي افتد. اين رسوب سنگين ممكن است در ديسپرسيون مجدد نيز اشكالاتي توليد كند. اين اشكالات مربوط به رواني و سياليت و رسوب رنگدانه را مي توان با تنظيم گرانروي رنگ از بين برد. به وسيله انتخاب صحيح رنگدانه ها مي توان كنترلهاي بيشتري براي جلوگيري از رسوب بكار برد.
گرانروي رنگ مي تواند به وسيله افزودن مواد ضخيم كننده و غليظ كننده افزايش داده شود، (يعني سياليت و رواني رنگ كم شود)، بدون اينكه حالت تيكسوتروپي در رنگ به وجود بيايد. عوامل ايجاد كننده حالت تيكسوتروپي، به رنگ ساختمان ژل مانندي مي دهد. اين حالت ژل مانند براي بسياري از رنگهائي كه به وسيله قلم مو مصرف مي شوند، مفيد است زيرا كه از سينه دادن و شره كردن آن جلوگيري مي نمايد. اين خاصيت نيز مي تواند مسئله رسوب در مدت نگهداري را كاهش داده و يا بطور كلي از بين ببرد.
رنگهائي كه حالت تيكسوتروپي دارند در تمام كاربردها مطلوب نيستند، براي مثال وقتي سياليت خوب مورد نظر است، در اين موقع نيز رسوب رنگدانه ها را مي توان با مواد ضد رسوب يا فعال كننده سطح مانند سويالستين در حدود 1 درصد فرمول بندي كاهش داد. مواد فعال كننده سطح به سطح رنگدانه جذب مي گردد كه در نتيجه باعث افزايش حجم و كاهش وزن مخصوص آن مي شود. نتيجه نهائي كاهش ميزان رسوب است. ديسپرسيون مجدد رنگدانه هاي رسوب كرده به وسيله استفاده از رنگدانه يارهاي فعال شده تسهيل مي گردد، كه معمولا اين رنگدانه يار، كربنات كلسيم به ميزان 5 درصد وزن رنگدانه مي باشد. ذرات اين رنگدانه يارها به دليل دارا بودن لايه سطح آلي بسيار پرحجم مي باشد و در خلال رسوب ذرات بين ذرات رنگدانه مستقر مي شوند. وقتي رنگ بهم زده مي شود ذرات رنگدانه يار به شكستن تجمع رنگدانه كمك مي كند و در نتيجه ديسپرسيون مجدد به راحتي انجام مي شود.
بسياري از مواد، گرانروي رنگ را افزايش مي دهند و يا موجب بوجود آمدن حالت تيكسوتروپي در فرمول بندي مي گردند. متداولترين انواع اين مواد عبارتند از : اترهاي سلولز، سيليكاهاي ميكرونيزه ، پنتونيتها
مواد ضد كف و كف زدا :
كف سيستمي متشكل از دو فاز گاز و مايع مي باشد كه فاز گاز در فاز مايع پخش شده است. هنگام كار با دستگاههاي مخلوط كني و پر كردن رنگ كف ايجاد مي شود و اين مسئله موجب كند شدن سرعت توليد، مسدود شدن پمپها و لوله ها و افزايش هزينه توليد رنگ مي گردد. لذا، بايد در زمان توليد رنگ موادي به آن افزود كه بتوان يا مانع ايجاد كف شد و يا اينكه آن را از بين برد. اين مواد را تحت عنوان «مواد ضد كف» و يا «مواد كف زدا» مي شناسند اما از نظر دسته بندي كلي مواد افزودني رنگ مي توان آنها را جزء «مواد فعال كننده سطح» بشمار آورد.
انتخاب مناسبترين و موثرترين ماده كف زدا يا ضد كف يك مسئله نسبتاً مشكل مي باشد، اما، قوانين زير، هر چند كه ثابت نيستند، مي توانند كمك زيادي به اين امر كنند :
1- كشش سطحي ضد كف بايد از كشش سطحي محلول كف كننده كمتر باشد
2- ضد كف بايد در محلول كف كننده قابليت حلاليت پائيني داشته باشد
3- ضد كف بايد با محلول كف كننده به آساني پخش شود
4- ضد كف بايدب ا محلول كننده واكنشي انجام ندهد
5- ضد كف بايد ضريب گسترش بالائي داشته باشد
6- ضد كف نبايد اثرات زيان آوري در محصول نهائي ايجاد كند
7- در مواردي كه داشتن بو يا مزه مهم باشد، ضد كف نبايد بو يا مزه خاصي از خود بجاي بگذارد
8- ضد كف نبايد موجب تجمع رنگدانه و ناپايداري امولسيون شود
9- ضد كف بايد با مخلوط كف كننده امتزاج پذيري خوبي داشته باشد تا از پيدايش معايبي از قبيل چشم ماهي شدن يا ژل شدن فيلم خشك نشده رنگ جلوگيري شود
10- ضد كف بايد فعاليت خود را براي يك زمان طولاني حفظ كند.
لازم به تذكر استكه علاوه بر عوامل فوق، عوامل ديگري از قبيل گرانروي و ساير اجزاي متشكله رنگ، دماف سرعت فرايند توليد نيز در كارائي ماده ضد كف يا كف زدا موثر هستند.
مهمترين مواد ضد كف يا كف زداي مصرفي سيليكونها، بعضي الكلهاي شش الي ده كربنه (مثلا تونيل الكل)، مشتقات پلي اتيلن اكسايد و پلي پروپلين اكسايد و بعضي از محصولات طبيعي مانند ترپنتين، روغن كاج و روغن پشم و غيره مي باشد. از آنجا كه خواص ضد كف در فرمول بنديهاي گوناگون متفاوت است نوع و مقدار قابل استفاده هر يك از اين مواد يكسان نيست. پيشنهاد مي شود كه براي استفاده از نوع و ميزان مصرف هر يك از مواد ضد كف يا كف زدا از توصيه ها و اطلاعات سازندگان آنها كمك گرفته شود. معمولا سازندگان اين گونه مواد درصد ماده فعال موجود در آنها را چنان تنظيم مي كنند كه حدود 1/0 تا 5/0 درصد از كل وزن رنگ را بخود اختصاص دهند.
آب بدليل كشش سطحي و قطبيت بالا فاز مايع مناسبي براي ايجاد كف بشمار مي آيد، لذا در ساخت رنگهاي امولسيوني استفاده از مواد ضد كف بسيار ضروري و مفيد مي باشد. رنگهاي ساخته شده از رزينهاي امولسيون آكريليك ، پلي وينيل استات ، پلي وينيل الكل ، آلكيد و كائوچو نياز حتمي به اينگونه مواد دارند.
در صنعت رنگسازي تفاوت زيادي بين مواد ضد كف و كف زدا وجود ندارد و هر دو تحت يك عنوان به فروش مي رسند. از مواد ضد كف در توليداتي كه هدف جلوگيري از تشكيل كف است استفاده مي شود و در صورتي كه مواد كف زدا هنگامي استفاده مي شوند كه منظور از بين بردن كف توليد شده است.
يكي از روشهاي عمومي در صنعت رنگسازي اين است كه نصف مواد ضد كف مورد نظر را ضمن پخش كردن رنگدانه به مخلوط رنگ مي افزايند تا از تشكيل كف جلوگيري شود. سپس بقيه مواد ضد كف را در مرحله همرنگ كردن رنگ جهت عدم تشكيل كف بيشتر در هنگام پركردن قوطيها و استعمال رنگ اضافه مي كنند. البته استفاده از دو نوع ماده ضد كف هم منطقي بنظر مي آيد، زيرا ممكن است يكي از آنها در شرايط سخت پخش رگدانه موثرتر باشد و ديگري در شرايط نگهداري طولاني مدت رنگ مفيدتر واقع شود.
مواد مقاوم كننده فيلم رنگ در مقابل رطوبت
نفوذ آب به درون فيلم رنگها شامل فرايندهاي پخش و جذب آب توسط فيلم رنگ مي باشد، اما هيچر ابطه مستقيمي بين ميزان آب نفوذ كرده و آب جذب شده وجود ندارد. بعضي از مواد آلي با وجود اينكه مقدار قابل توجهي آب از خود عبور مي دهند (يعني به درون آنها نفوذ مي كند اما تنها مقدرا بسيار ناچيزي از آن را جذب مي كنند، و ممكن است در برخي موارد عكس اين مسئله مشاهده شود. جذب آب توسط شيبي موجب ورم كردن آن شده و ممكن است بر روي ساختمان فيزيكي آن اثر بگذارد. درفيلم بعضي از رنگها جذب آب منجر به تغييراتي در قابليت نفوذ آنها در مقابل رطوبت و ديگر اجزاي متشكله محيط اطراف مي گردد. بعضي از رنگها در نتيجه جذب آب استحكام و چسبندگي خود را از دست مي دهند، بطوري كه حتي پس از رفع رطوبت نيز هرگز استحكام و چسبندگي اوليه خود را باز نمي يابند، در حالي كه برخي ديگر از رنگها مي توانند ميزان قابل توجهي رنگ جذب كنند بدون اينكه اثر محسوسي بر روي خصوصيات و عملكرد آنها داشته باشد.
ميزان ورم كردن فيلم رنگ در نتيجه جذب آب عمدتا به طبيعت اجزاي متشكله آن فيلم بستگي دارد. وجود گروههاي هيدروكسيل و ديگر گروههاي قطبي، و افزودن اجزايي كه وزن مولكولي پائيني دارند و قابل حل در آب هستند، كلا موجب تسريع در ورم كردن لايه رنگ مي شوند. تورم در آب تنها يكي از ملاكهاي تعيين كننده مقاومت در مقابل رطوبت مي باشد، و در همه موارد ميزان آب نفوذ كرده به درون فيلم رنگ را نشان نمي دهد. همانطور كه اشاره شد، فيلم برخي از رنگها در نتيجه جذب آب ورم مي كنند، اما اجازه عبور آب از درون خود را نمي دهند، برعكس،بعضي ديگر ورم نمي كنند اما به آساني از درون آنها عبور مي كند (مانند استرهاي سلولز و غيره)
بنابراين، نفوذ رطوبت به درون فيلم رنگها تحت تاثير اجزاي متشكله فيلم رنگ (يعني نوع رنگپايه و رنگدانه مصرفي) قرار دارد. رزينهاي وينيلي كه رايجترين رزينها مي باشند مقاومت خوبي در مقابل نفوذ رطوبت دارا نيستند، با وجود اين، مي توان با استفاده از تري كرسيل فسفات، كه هم به عنوان نرم كننده عمل مي كند و هم به عنوان يك ماده كمكي براي افزايش مقاومت درمقابل نفوذ آب، اين نقيصه را تا حدودي برطرف كرد.
مواد ضد يخ :
وقتي كه يك رنگ حاوي آب (رنگي كه حلال آن آب است ) در درجات حرارت پائين قرار مي گيرد، منجمد مي شود. يخ زدن رنگهاي آبي زيان مهمي به رنگ وارد نمي كند، مگر آنكه حجم نسبتا زيادي از آن يخ بزند كه در اين صورت موجب باز كردن ظرف محتوي رنگ مي گردد. با وجود اين، در يك سيستم امولسيوني ، مثلا يك سيستم امولسيوني متشكل از آب و روغن؛ وقتي كه فاز اصلي را آب تشكيل دهد، انجماد باعث تشكيل بلورهاي يخ و در نتيجه دلمه بستن بخشي از رزين موجود در سيستم مي شود. هر قدر عمل انجماد آهسته تر صورت گيرد بلوهراي تشكيل شده يخ بزرگتر بوده و در نتيجه زيان حاصل از دلمه بستن رزين بيشتر خواهد بود. در يك سيتسم امولسيوني هر قدر ميزان رنگدانه مصرفي بيشتر باشد، زيانهاي ناشي از انجماد كمتر خواهد بود. رنگي كه ميزان رنگدانه آن كم مي باشد ممكن است در نتيجه انجماد به صورت دلمه در آيد، در حالي كه اگر ميزان رنگدانه آن بالا باشد ممكن است انجماد تنها قدري گرانروي آن را افزايش دهد. آثار سوء انجماد بر روي خصوصيات رنگهاي آبي ممكن است با آب شدن يخ قابل بر طرف شدن باشد، اما مسئله مهم دلمه بستن رزين موجود در رنگ است كه در شرايط عادي اين اثر بخصوص در يك سيستم امولسيوني، برگشت پذير نبوده و در نتيجه بازيابي لاتكس يا رنگ منجمد شده غير ممكن خواهد بود، لذا لازم است كه رد ساخت رنگهاي آبي از مواد ضد يخ استفاده كرد. رايجترين مواد ضد يخ مصرفي در صنعت رنگ، گليكولها مي باشند، كه تركيبات آلي سير شده خطي با دو گروه هيدروكسيل هستند. گليكولها اساسا مايعاتي شفاف، بيرنگ و تقريبا بي بو مي باشند و در نتيجه مي توان گفت كه از نظرخصوصيات ظاهري تقريبا شبيه آب هستند. با وجود اين، در هر درجه حرارتي سنگينتر و غليظ تر از آب مي باشند و نقاط جوش بسيار بالاتري دارند.
بدون شك اتيلن گليكول رايجترين ماده ضدي خي است كه در رنگهاي لاتكس مصرف مي شود. ميزان مصرف عادي آن 15 تا 20 پوند در يكصد گالن مي باشد، اما، گاهي اوقات ممكن است اين ميزان مصرف تا 40 پوند نيز برسد. پروپيلن گيلكول دومين گليكول مصرفي در صنعت رنگ مي باشد و چون كمي ارزانتر از اتيلن گيلكول است و تاثير سوء چنداني بر روي خصوصيات رنگ ندارد، اغلب به عنوان جايگزين اتيلن گيلكول مورد استفاده قرار مي گيرد. ديگر گليكولهائي كه در موارد خاص در رنگهاي لاتكس بكار مي رود پلي پروپيلن گليكول، دي اتيلن گليكول، هگزيلن گليكول و گليسيرين مي باشند.
مواد كنترل كننده برق فيلم رنگ (مواد مات كننده) :
براقيت را بايد به عنوان خصوصيتي از يك سطح دانست كه نور را همانند يك آينه منعكس مي كند. با توجه به اين تعريف، منظور از حفظ براقيت توانايي فيلم رنگ براي نگهداري براقيت اوليه مي باشد. در نتيجه، اگر رنگي براقيت خود را به مدت نامحدودي حفظ كند مي گويند قدرت حفظ برق عالي دارد و اگر برق خود را بسرعت از دست بدهد مي گويند قدرت حفظ برق آن ضعيف است.
دو عامل مهم در براقيت فيلم رنگ، نوع رنگپايه و رنگدانه مصرفي در آن مي باشد. اما، براي كنترل برق فيلم رنگ از مواد افزودني خاصي نيز استفاده مي شود كه بعضي از آنها موجب كاهش برق (مواد مات كننده) و بعضي ديگر موجب افزايش برق مي گردند.
امروزه انواع بسيار ريز سيليكاها (دي اكسيد سيليكون) به عنوان يك ماده مات كننده عمومي مورد قبول قرار گرفته اند، اما بعضي از انواع آنها كه شديداً اسيدي هستند براي استفاده در لاكهاي وينيلي يا پوششهاي اوره- آلكيد كاتاليز شده با اسيد مناسب نيستند، زيرا بر روي پايداري سيستم اثر مي گذارند. استئارات روي نيز از جمله مواد مات كننده مصرفي در صنايع رنگسازي است. استئارات كلسيم يك ماده كننده خوب براي رنگها، روغن هاي جلا و لاكها، به خصوص براي مواردي كه گرانروي پايين مورد نظر است مي باشد.
برچسب : نویسنده : علیرضا فرزادنیا chemis بازدید : 244 تاريخ : دوشنبه 2 فروردين 1389 ساعت: 21:0
آرشیو مطالب
- اسفند 1386
- مهر 1386
- آبان 1386
- دی 1387
- بهمن 1387
- اسفند 1387
- فروردين 1387
- خرداد 1387
- مهر 1387
- آبان 1387
- آذر 1387
- بهمن 1388
- اسفند 1388
- فروردين 1388
- ارديبهشت 1388
- خرداد 1388
- تير 1388
- شهريور 1388
- آبان 1388
- بهمن 1389
- اسفند 1389
- فروردين 1389
- ارديبهشت 1389
- خرداد 1389
- تير 1389
- شهريور 1389
- مهر 1389
- آبان 1389
- دی 1390
- بهمن 1390
- اسفند 1390
- فروردين 1390
- ارديبهشت 1390
- خرداد 1390
- مرداد 1390
- شهريور 1390
- مهر 1390
- آبان 1390
- آذر 1390
- دی 1391
- بهمن 1391
- اسفند 1391
- فروردين 1391
- ارديبهشت 1391
- تير 1391
- مرداد 1391
- شهريور 1391
- مهر 1391
- آبان 1391
- آذر 1391
- بهمن 1392
- اسفند 1392
- فروردين 1392
- تير 1392
- مرداد 1392
- شهريور 1392
- آبان 1392


